你可能感兴趣的试题
该电池不适宜在过高或过低温度下使用 正极反应中有CO2生成 质子通过交换膜从负极区移向正极区 电池总反应为C6H12O6+ 6O2==6CO2 +6H2O
正极反应中有CO2生成 微生物促进了反应中电子的转移 质子通过交换膜从负极区移向正极区 电池总反应为C6H12O6+6O2=6CO2+6H2O
A极电极反应式为: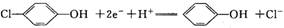 B.极电极反应式为:CH3COO--8e-+4H2O=2HCO3-+9H+ 溶液中的阴离子由A.极向B.极移动 该微生物电池在高温条件下无法正常工作1.
B.极电极反应式为:CH3COO--8e-+4H2O=2HCO3-+9H+ 溶液中的阴离子由A.极向B.极移动 该微生物电池在高温条件下无法正常工作1.
电流方向从 极沿导线经小灯泡流向A.极 B.A极的电极反应式为  当外电路中有0.2mole-转移时,正极消耗的H+的个数为0.2NA B为电池的正极,发生还原反应
当外电路中有0.2mole-转移时,正极消耗的H+的个数为0.2NA B为电池的正极,发生还原反应
正极反应中有CO2生成 微生物促进了反应中电子的转移[学 质子通过交换膜从负极区移向正极区 电池总反应为C6H12O6+6O2=6CO2+6H2O
正极反应中有CO2生成 微生物促进了反应中电子的转移 质子通过交换膜从负极区移向正极区 电池总反应为C6H12O6+6O2=6CO2+6H2O
b极为正极,发生还原反应 一段时间后b极区电解液的pH减小 H+由a极穿过质子交换膜到达b极 a极的电极反应式为 -e-=Cl-+
-e-=Cl-+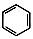
正极反应中有CO2生成 微生物促进了反应中电子的转移 质子通过交换膜从负极区移向正极区 电池总反应为C6H12O6+6O2═6CO2+6H2O
正极反应中有CO2生成 微生物促进了反应中电子的转移 质子通过交换膜从负极区移向正极区 电池总反应为C6H12O6+6O2===6CO2+6H2O
X.极为微生物电池的负极 该电池能够在高温下工作 图中离子交换膜应为阴离子交换膜 Y.极电极反应式为:CH3COO--8e-+4H2O=2HCO3-+9H+
正极反应中有CO2生成 微生物促进了反应中电子的转移 质子通过交换膜从负极区移向正极区 电池总反应为C6H12O6+6O2===6CO2+6H2O
正极反应中有CO2生成 微生物促进了反应中电子的转移 质子通过交换膜从负极区移向正极区 电池总反应为C6H12O6+6O2===6CO2+6H2O
该电池不适宜在过高或过低温度下使用 正极反应中有CO2生成 质子通过交换膜从负极区移向正极区 电池总反应为C6H12O6+ 6O2==6CO2 +6H2O
正极反应中有CO2生成 微生物促进了反应中电子的转移 质子通过交换膜从负极区移向正极区 电池总反应为C6H12O6+6O2=6CO2+6H2O

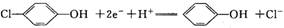 B.极电极反应式为:CH3COO--8e-+4H2O=2HCO3-+9H+ 溶液中的阴离子由A.极向B.极移动 该微生物电池在高温条件下无法正常工作1.
B.极电极反应式为:CH3COO--8e-+4H2O=2HCO3-+9H+ 溶液中的阴离子由A.极向B.极移动 该微生物电池在高温条件下无法正常工作1.
 当外电路中有0.2mole-转移时,正极消耗的H+的个数为0.2NA B为电池的正极,发生还原反应
当外电路中有0.2mole-转移时,正极消耗的H+的个数为0.2NA B为电池的正极,发生还原反应
 -e-=Cl-+
-e-=Cl-+