你可能感兴趣的试题
在一定浓度下,平衡常数值越大则酸的电离度也越大 在一定浓度下,平衡常数值越大则酸的电离度越小 平衡常数值越大则溶液的浓度越大 平衡常数值越大则溶液的浓度越小
电离平衡常数能衡量电解质电离的相对强弱 电离平衡常数不随浓度变化而变化 电离平衡常数与温度有关 电离平衡常数不随任何条件而改变
电离平衡常数受溶液浓度的影响 电离平衡常数可以表示弱电解质的相对强弱 电离常数大的酸溶液中c(H+)一定比电离常数小的酸中大 H2CO3的电离常数表达式:K= 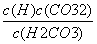
HF的电离平衡常数为7.2×10-4 HNO2的电离平衡常数为4.9×10-10 根据①③两个反应即可知三种酸的相对强弱 HNO2的电离平衡常数比HCN大,比HF小
在18℃时溶解度比25℃时小 的电离是一个吸热过程 温度高时电离度变小 温度高时溶液中的氢离子浓度变小
电离平衡常数可以表示弱电解质的相对强弱 电离平衡常数受溶液浓度的影响 H2CO3的电离常数表达式:K.= 电离常数大的酸溶液中c(H+)一定比电离常数小的酸中大
电离常数大的酸溶液中c(H+)一定比电离常数小的酸中大
HF的电离平衡常数为7.2×10﹣4 HNO2的电离平衡常数为4.9×10﹣10 根据①③两个反应即可知三种酸的相对强弱 HNO2的电离平衡常数比HCN大,比HF小
在18℃时溶解度比25℃时小 的电离是一个放热过程 温度高时电离度变大 温度低时溶液中的氢离子浓度变大
在一定浓度下,平衡常数值越大则酸的电离度也越大 在一定浓度下,平衡常数值越大则酸的电离度越小 平衡常数值越大则溶液的浓度越大 平衡常数值越大则溶液的浓度越小
HF的电离平衡常数为7.2×10-4 HNO2的电离平衡常数为4.9×10-10 根据①③两个反应即可知三种酸的相对强弱 HNO2的电离平衡常数比HCN大,比HF小
电离平衡常数能衡量电解质电离的相对强弱 电离平衡常数不随浓度变化而变化 电离平衡常数与温度有关 电离平衡常数不随任何条件而改变
在18℃时溶解度比25℃时小 电离是一个放热过程 温度高时电离度变大 温度低时溶液中的氢离子浓度变大
在18℃时溶解度比25℃时小 的电离是一个吸热过程 温度高时电离度变大 温度高时溶液中的氢离子浓度变小
电离平衡常数能衡量电解质电离的相对强弱 电离平衡常数不随浓度的变化而变化 电离平衡常数与温度有关 电离平衡常数不随任何条件而改变
HF的电离平衡常数为7.2×10-4 HNO2的电离平衡常数为4.9×10-10 根据①③两个反应即可知三种酸的相对强弱 HNO2的电离平衡常数比HCN大,比HF小
电离平衡常数受溶液浓度的影响 电离平衡常数可以表示弱电解质的相对强弱 电离常数大的酸溶液中c(H+)一定比电离常数小的酸中大 H2CO3的电离常数表达式:K.=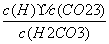
在18℃时溶解度比25℃小 的电离过程是放热过程 温度高时电离度变大 温度低时溶液中的氢离子浓度变大
HNO2的电离平衡常数是③ HNO2的电离平衡常数是① HCN的电离平衡常数是② HF的电离平衡常数是①
电离度越大,电离平衡常数越大; 浓度越稀,电离度越大,电离平衡常数越大; 在相同的温度下电离度可变,而电离平衡常数不变; 多元弱酸的每一步电离平衡常数是相同的
HF的电离平衡常数为7.2×10-4 HNO2的电离平衡常数为4.9×10-10 根据①③两个反应即可知三种酸的相对强弱 HNO2的电离平衡常数比HCN大,比HF小

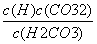
 电离常数大的酸溶液中c(H+)一定比电离常数小的酸中大
电离常数大的酸溶液中c(H+)一定比电离常数小的酸中大