V 变压器输出端交变电流的频率为50Hz 变压器的输出功率为220
V 变压器输出端交变电流的频率为50Hz 变压器的输出功率为220 W
W 
 (V.) R.′减小时,电流表的示数变大,电压表V2的示数变大 变压器原线圈的输入功率和副线圈的输出功率之比为55∶9
(V.) R.′减小时,电流表的示数变大,电压表V2的示数变大 变压器原线圈的输入功率和副线圈的输出功率之比为55∶9




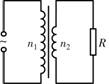




 W 电压表的示数是100
W 电压表的示数是100 V
V 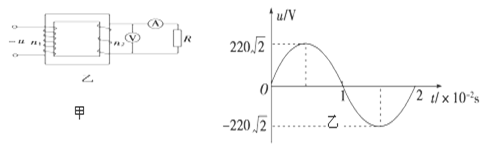
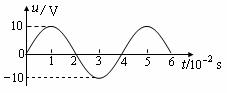
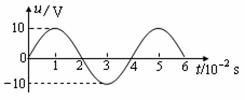
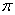 t)V. 该交变电压有效值约为7.1V 将该交变电压接在匝数比为1∶2的理想变压器原线圈上,副线圈输出频率为50 Hz 将该交变电压加在阻值R=20 Ω的白炽灯两端,电灯消耗的功率是5W
t)V. 该交变电压有效值约为7.1V 将该交变电压接在匝数比为1∶2的理想变压器原线圈上,副线圈输出频率为50 Hz 将该交变电压加在阻值R=20 Ω的白炽灯两端,电灯消耗的功率是5W