你可能感兴趣的试题
1 mol N2(g)和1 mol O2(g)反应放出的能量为180 kJ 1 molN2(g)和1 mol O2(g)具有的总能量小于2 mol NO(g)具有的总能量 通常情况下,N2(g)和O2(g)混合能直接生成NO NO是一种酸性氧化物,能与NaOH溶液反应生成盐和水
1mL酒精和1mL水混合后的总体积 1g金属铁和1g稀盐酸反应后溶液的质量 1g氢氧化钠溶液和1g盐酸溶液混合后溶液的质量 1g饱和食盐水中加入1g食盐后,所得溶液的质量
1 mol N2(g)和1 mol O2(g)反应放出的能量为180 kJ 1 mol N2(g)和1 mol O2(g)具有的总能量小于2 mol NO(g)具有的总能量 通常情况下,N2(g)和O2(g)混合能直接生成NO NO是一种酸性氧化物,能与NaOH溶液反应生成盐和水
(g)+ (g)  (g)+ (g)过程中的能量变化如图所示,由此可判断 A.1molA与1molB充分反应后,能量变化为ΔE B.加入催化剂后,反应加快,ΔE减小 C.反应物的总键能小于生成物的总键能 D.反应达到平衡时,升高温度,A.的转化率增大
(g)+ (g)过程中的能量变化如图所示,由此可判断 A.1molA与1molB充分反应后,能量变化为ΔE B.加入催化剂后,反应加快,ΔE减小 C.反应物的总键能小于生成物的总键能 D.反应达到平衡时,升高温度,A.的转化率增大 
(g)+B(g)→C(g) △H.,分两步进行:①A.(g)+B(g)→X(g)△H1,②X(g) →C(g)△H2, 反应过程中能量变化如图所示,E1表示A.+B→X的活化能,下列说法正确的是( ) 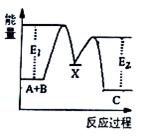 A. △H1=△H.一△H2>0 X.是反应A.(g)+B(g)→C(g)的催化剂 E2是反应②的活化能 △H1=E1-E2
A. △H1=△H.一△H2>0 X.是反应A.(g)+B(g)→C(g)的催化剂 E2是反应②的活化能 △H1=E1-E2
图中a、b曲线可分别表示反应 CH2=CH2(g)+H2(g)→CH3CH3(g) ΔH.<0 使用和未使用催化剂时,反应过程中的能量变化 己知2C(s)+2O2(g)=2CO2(g) ΔH.1; 2C(s)+O2(g)=2CO(g) ΔH.2。则ΔH.1>ΔH.2 同温同压下,反应H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的ΔH.不同 在一定条件下,某可逆反应的ΔH.=+100kJ·mol-1,则该反应正反应活化能比逆反应活化能大100kJ·mol-1
在一定条件下,某可逆反应的△H=+100kJ•mol-1,则该反应正反应活化能比逆反应活化能大100kJ•mol-1 图中A.B.曲线可分别表示反应: CH2=CH2(g)+H2(g)→CH3CH3(g)△H.>0 未使用和使用催化剂时,反应过程中的能量变化 同温同压下,反应H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件 下的△H.不同 己知2C(s)+2O2(g)=2CO2(g)△H1;2C(s)+O2(g)=2CO(g)△H2.则△H1>△H2
(g)+B(g)⇌C.(g)+D(g)过程中的能量变化如图所示,下列说法正确的是( ) A.该反应是放热反应 加入催化剂后,反应加快,△H.减小 反应物的总键能小于生成物的总键能 反应达到平衡时,升高温度,A.的转化率增大
反应物的总键能小于生成物的总键能 反应达到平衡时,升高温度,A.的转化率增大
(g)+ (g)―→C(g) ΔH.,分两步进行:  ①A(g)+B.(g)―→X(g) ΔH.1 ②X(g)―→C(g) ΔH.2 反应过程中能量变化如下图所示,E.1表示A.+B―→X的活化能。下列说法正确的是( ) A.ΔH.1=ΔH.-ΔH.2>0 B.X.是反应A.(g)+B.(g)―→C(g)的催化剂 E.2是反应②的活化能 ΔH.=E.1-E.2
①A(g)+B.(g)―→X(g) ΔH.1 ②X(g)―→C(g) ΔH.2 反应过程中能量变化如下图所示,E.1表示A.+B―→X的活化能。下列说法正确的是( ) A.ΔH.1=ΔH.-ΔH.2>0 B.X.是反应A.(g)+B.(g)―→C(g)的催化剂 E.2是反应②的活化能 ΔH.=E.1-E.2
(g)+ (g)  (g)+ (g)过程中的能量变化如图所示, ①正反应为放热反应, ②反应物总能量低于生成物总能量, ③反应物的总键能小于生成物的总键能, ④1molA与1molB充分反应后,能量变化为ΔE, ⑤加入催化剂后,反应加快,ΔE减小, ⑥反应达到平衡时,升高温度,A.的转化率增大, ⑦升高温度可增大正反应速率,降低逆反应速率, ⑧E.2是反应C.(g)+D.(g)
(g)+ (g)过程中的能量变化如图所示, ①正反应为放热反应, ②反应物总能量低于生成物总能量, ③反应物的总键能小于生成物的总键能, ④1molA与1molB充分反应后,能量变化为ΔE, ⑤加入催化剂后,反应加快,ΔE减小, ⑥反应达到平衡时,升高温度,A.的转化率增大, ⑦升高温度可增大正反应速率,降低逆反应速率, ⑧E.2是反应C.(g)+D.(g)  A.(g)+B.(g) 的活化能, 以上有关说法正确的是 A.⑤⑥⑦⑧B.①②③④C.①③⑤⑦D.②⑥⑧
A.(g)+B.(g) 的活化能, 以上有关说法正确的是 A.⑤⑥⑦⑧B.①②③④C.①③⑤⑦D.②⑥⑧
在一定条件下,某可逆反应的△H=+100kJ•mol-1,则该反应正反应活化能比逆反应活化能大100kJ•mol-1 图中A.B.曲线可分别表示反应: CH2=CH2(g)+H2(g)→CH3CH3(g)△H.>0 未使用和使用催化剂时,反应过程中的能量变化 同温同压下,反应H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件 下的△H.不同 己知2C(s)+2O2(g)=2CO2(g)△H1;2C(s)+O2(g)=2CO(g)△H2.则△H1>△H2
(g)+ (g)―→C(g) ΔH,分两步进行:①A(g)+B.(g)―→X(g) ΔH1; ②X(g)―→C(g) ΔH2。反应过程中能量变化如图1所示, E1表示A.+B―→X的活化能,下列说法正确的是 A.ΔH1=ΔH-ΔH2>0 B.X.是反应A.(g)+B.(g)―→C(g)的催化剂 E2是反应②的活化能 ΔH=E1-E2
1 mol N2(g)和1 mol O2(g)反应放出的能量为180 kJ 1 mol N2(g)和1 mol O2(g)具有的总能量小于2 mol NO(g)具有的总能量 通常情况下,N2(g)和O2(g)混合能直接生成NO NO是一种酸性氧化物,能与NaOH溶液反应生成盐和水
NO能与NaOH反应生成盐和水 通常N2(g)和O2(g)混合能直接生成NO(g) 当有1molNO(g)生成时,反应吸收的能量为90kJ 1molN2(g)和1mol O2(g)具有的总能量 大于2molNO(g)具有的总能量
1 mol N2(g)和1 mol O2(g)反应放出的能量为180 kJ 1 mol N2(g)和1 mol O2(g)具有的总能量小于2 mol NO(g)具有的总能量 通常情况下,N2(g)和O2(g)混合能直接生成NO NO是一种酸性氧化物,能与NaOH溶液反应生成盐和水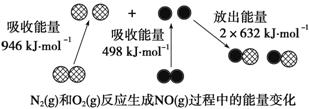
(g)+B(g)=C(g)△H,分两步进行:  ①A(g)+B(g)=X(g)△H1 ②X(g)=C(g)△H2 反应过程中能量变化如图所示,E1表示A.+B=X的活化能,下列说法正确的是( ) A.△H=E1-E2 X.是反应A.(g)+B(g)= (g)的催化剂 C.E2是反应②的活化能 △Hl=△H-△H2>0
①A(g)+B(g)=X(g)△H1 ②X(g)=C(g)△H2 反应过程中能量变化如图所示,E1表示A.+B=X的活化能,下列说法正确的是( ) A.△H=E1-E2 X.是反应A.(g)+B(g)= (g)的催化剂 C.E2是反应②的活化能 △Hl=△H-△H2>0
1mol N2(g)和1mol O2(g)反应放出的能量为180kJ 1mol N2(g)和1mol O2(g)具有的总能量小于2mol NO (g)具有的总能量 通常情况下,N2(g)和 O2(g)混合能直接生成NO (g) NO是一种酸性氧化物,能与NaOH溶液反应生成盐和水
1g酒精和1g水混合后的总质量 1g金属铁和1g稀盐酸反应后溶液的质量 1g饱和食盐水中加入1g食盐后,所得溶液的质量 1g氢氧化钠溶液和1g醋酸溶液混合后溶液的质量
(g)+ (g)  (g)+ (g)过程中的能量变化如图所示,由此可判断( ) A.1molA与1molB充分反应后,能量变化为ΔE B.加入催化剂后,反应加快,ΔE减小 C.反应物的总键能小于生成物的总键能 D.反应达到平衡时,升高温度,A.的转化率增大
(g)+ (g)过程中的能量变化如图所示,由此可判断( ) A.1molA与1molB充分反应后,能量变化为ΔE B.加入催化剂后,反应加快,ΔE减小 C.反应物的总键能小于生成物的总键能 D.反应达到平衡时,升高温度,A.的转化率增大

 (g)+ (g)过程中的能量变化如图所示,由此可判断 A.1molA与1molB充分反应后,能量变化为ΔE B.加入催化剂后,反应加快,ΔE减小 C.反应物的总键能小于生成物的总键能 D.反应达到平衡时,升高温度,A.的转化率增大
(g)+ (g)过程中的能量变化如图所示,由此可判断 A.1molA与1molB充分反应后,能量变化为ΔE B.加入催化剂后,反应加快,ΔE减小 C.反应物的总键能小于生成物的总键能 D.反应达到平衡时,升高温度,A.的转化率增大 
 A. △H1=△H.一△H2>0 X.是反应A.(g)+B(g)→C(g)的催化剂 E2是反应②的活化能 △H1=E1-E2
A. △H1=△H.一△H2>0 X.是反应A.(g)+B(g)→C(g)的催化剂 E2是反应②的活化能 △H1=E1-E2
 反应物的总键能小于生成物的总键能 反应达到平衡时,升高温度,A.的转化率增大
反应物的总键能小于生成物的总键能 反应达到平衡时,升高温度,A.的转化率增大
 ①A(g)+B.(g)―→X(g) ΔH.1 ②X(g)―→C(g) ΔH.2 反应过程中能量变化如下图所示,E.1表示A.+B―→X的活化能。下列说法正确的是( ) A.ΔH.1=ΔH.-ΔH.2>0 B.X.是反应A.(g)+B.(g)―→C(g)的催化剂 E.2是反应②的活化能 ΔH.=E.1-E.2
①A(g)+B.(g)―→X(g) ΔH.1 ②X(g)―→C(g) ΔH.2 反应过程中能量变化如下图所示,E.1表示A.+B―→X的活化能。下列说法正确的是( ) A.ΔH.1=ΔH.-ΔH.2>0 B.X.是反应A.(g)+B.(g)―→C(g)的催化剂 E.2是反应②的活化能 ΔH.=E.1-E.2
 (g)+ (g)过程中的能量变化如图所示, ①正反应为放热反应, ②反应物总能量低于生成物总能量, ③反应物的总键能小于生成物的总键能, ④1molA与1molB充分反应后,能量变化为ΔE, ⑤加入催化剂后,反应加快,ΔE减小, ⑥反应达到平衡时,升高温度,A.的转化率增大, ⑦升高温度可增大正反应速率,降低逆反应速率, ⑧E.2是反应C.(g)+D.(g)
(g)+ (g)过程中的能量变化如图所示, ①正反应为放热反应, ②反应物总能量低于生成物总能量, ③反应物的总键能小于生成物的总键能, ④1molA与1molB充分反应后,能量变化为ΔE, ⑤加入催化剂后,反应加快,ΔE减小, ⑥反应达到平衡时,升高温度,A.的转化率增大, ⑦升高温度可增大正反应速率,降低逆反应速率, ⑧E.2是反应C.(g)+D.(g)  A.(g)+B.(g) 的活化能, 以上有关说法正确的是 A.⑤⑥⑦⑧B.①②③④C.①③⑤⑦D.②⑥⑧
A.(g)+B.(g) 的活化能, 以上有关说法正确的是 A.⑤⑥⑦⑧B.①②③④C.①③⑤⑦D.②⑥⑧


 ①A(g)+B(g)=X(g)△H1 ②X(g)=C(g)△H2 反应过程中能量变化如图所示,E1表示A.+B=X的活化能,下列说法正确的是( ) A.△H=E1-E2 X.是反应A.(g)+B(g)= (g)的催化剂 C.E2是反应②的活化能 △Hl=△H-△H2>0
①A(g)+B(g)=X(g)△H1 ②X(g)=C(g)△H2 反应过程中能量变化如图所示,E1表示A.+B=X的活化能,下列说法正确的是( ) A.△H=E1-E2 X.是反应A.(g)+B(g)= (g)的催化剂 C.E2是反应②的活化能 △Hl=△H-△H2>0
 (g)+ (g)过程中的能量变化如图所示,由此可判断( ) A.1molA与1molB充分反应后,能量变化为ΔE B.加入催化剂后,反应加快,ΔE减小 C.反应物的总键能小于生成物的总键能 D.反应达到平衡时,升高温度,A.的转化率增大
(g)+ (g)过程中的能量变化如图所示,由此可判断( ) A.1molA与1molB充分反应后,能量变化为ΔE B.加入催化剂后,反应加快,ΔE减小 C.反应物的总键能小于生成物的总键能 D.反应达到平衡时,升高温度,A.的转化率增大