你可能感兴趣的试题
图①表示25℃时,和0.1mol·L-1盐酸滴定20mL 0.1mol·L-1NaOH溶液 图②表示常温下,等量锌粉与足量的等体积等浓度的盐酸反应 图③表示向CaCl2和盐酸的混合溶液中滴加Na2CO3溶液 图④表示向盐酸和醋酸混合溶液中滴入氨水
向含有CaCO3沉淀的水中通入CO2至沉淀恰好溶解,再向溶液中加入NaHCO3饱和溶液, 又有CaCO3沉淀生成 向Na2 CO3溶液中逐滴加入等物质的量的稀盐酸,生成的CO2与原溶液中Na2CO3的物质 的量之比为1:2 等质量的NaHCO3和Na2 CO3分别与足量稀盐酸反应,在同温同压下,生成的CO2体积相同 向Na2CO3饱和溶液中通入足量CO2,有NaHCO3 结晶析出
在Na2CO3溶液中:c(OH-)-c(H+)=c(HCO3-)+c(H2CO3)
在pH=8的NaB溶液中:c(Na+)-c(B-)=9.9×10-7 mol/L
浓度均为0.1 mol/L的NaClO、NaHCO3混合溶液中:  c(HClO)+c(ClO-)=c(HCO3-) +c(H2CO3)
c(HClO)+c(ClO-)=c(HCO3-) +c(H2CO3)
向10mL pH=12的NaOH溶液中滴加pH=2的HA溶液达中性:则混合液体积V.总≥20mL
在0.1 mol/L Na2CO3溶液中: c(Na+)+c(H+)=c(CO32-)+c(HCO3-)+c(OH-) 当溶液的pH为7时,溶液的总体积为20 mL 在B.点所示的溶液中,浓度最大的阳离子是Na+ 在A.点所示的溶液中:c(CO32-)=c(HCO3-)>c(H+)>c(OH-)
向煮沸的1 molL-1NaOH溶液中滴加FeCl3饱和溶液制备Fe(OH)3胶体 向乙酸乙酯中加入饱和Na2CO3溶液,振荡,分液分离除去乙酸乙酯中少量乙酸 称取19.0 g SnCl2,用100 mL蒸馏水溶解,配制1.0 molL-1SnCl2溶液 用氢氧化铜粉末检测尿糖
在Na2CO3溶液中:c(OH﹣)﹣c(H+)═ c(HCO3﹣)+c(H2CO3) 在pH=8的NaB溶液中:c(Na+)﹣c(B.﹣)= 9.9×10﹣7 mol/L 浓度均为0.1 mol/L的NaClO、NaHCO3混合溶液中: c(HClO)+c(ClO﹣)═c(HCO3﹣)+c(H2CO3) 向10mL pH=12的NaOH溶液中滴加pH=2的HA溶液达中性:则混合液体积V.总≥20mL
在0.1mo1/L Na2CO3溶液中: 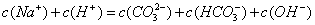 当溶液pH为7时,溶液的总体积为20mL 在B.点所示的溶液中,阳离子浓度最大的是Na 在A.点所示的溶液中:
当溶液pH为7时,溶液的总体积为20mL 在B.点所示的溶液中,阳离子浓度最大的是Na 在A.点所示的溶液中:
1000mL含Na2CO3212g 500mL含Na2CO3212g 1000mL含Na2CO3106g 500mL含Na2CO353g
在0.1mo1/L Na2CO3溶液中:  当溶液pH为7时,溶液的总体积为20mL 在B.点所示的溶液中,阳离子浓度最大的是Na 在A.点所示的溶液中:
当溶液pH为7时,溶液的总体积为20mL 在B.点所示的溶液中,阳离子浓度最大的是Na 在A.点所示的溶液中:
在Na2CO3溶液中:c(OH-)-c(H+)═c(HCO3-)+c(H2CO3) 在pH=8的NaB溶液中:c(Na+)-c(B-)=9.9×10-7 mol/L 浓度均为0.1 mol/L的NaClO、NaHCO3混合溶液中: c(HClO)+c(ClO-)═c(HCO3-)+c(H2CO3) 向10mLpH=12的NaOH溶液中滴加pH=2的HA溶液达中性,则混合溶液的体积 V.总≥20Ml
滴加过程中当溶液呈中性时,V(NaOH)>20mL 当V(NaOH)=30mL时,则有:2c(Na+)=3c(A2-)+3c(HA-) H2A在水中的电离方程式是:H2A.=H++HA-;HA-  H++A2- 当V(NaOH)=20mL时,则有:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(0H-)
H++A2- 当V(NaOH)=20mL时,则有:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(0H-) 
原NaOH溶液的浓度为0.lmol/L 通入CO2的体积为448mL 所得溶液的溶质成分的物质的量之比为(NaOH)∶(Na2CO3) =1∶3 所得溶液的溶质成分的物质的量之比为(NaHCO3)∶(Na2CO3) =2∶1
将1~2ml饱和FeCl3溶液逐滴滴到20ml 0.5 mol·L-1NaOH溶液中 将1~2ml饱和FeCl3溶液逐滴加入到20ml沸水中,并继续加热至溶液呈红褐色后停止加热 将1~2ml饱和FeCl3溶液逐滴加入到20ml冷水中,再加热至沸腾 将1~2ml沸水加入到1~2ml FeCl3饱和溶液中,并用玻璃棒不断搅拌
0.1 mol/L Na2CO3溶液中 c(Na+)+c(H+)=2c(CO32-)+c(HCO3-)+c(OH-) 在A.点:c(Na+)> c(CO32-)> c(HCO3-)> c(OH-)> c(H+) 常温下CO2饱和溶液的pH约为5.6 0.05 mol/L NaHCO3溶液的pH=8 

 c(HClO)+c(ClO-)=c(HCO3-) +c(H2CO3)
c(HClO)+c(ClO-)=c(HCO3-) +c(H2CO3)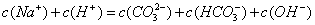 当溶液pH为7时,溶液的总体积为20mL 在B.点所示的溶液中,阳离子浓度最大的是Na 在A.点所示的溶液中:
当溶液pH为7时,溶液的总体积为20mL 在B.点所示的溶液中,阳离子浓度最大的是Na 在A.点所示的溶液中:
 当溶液pH为7时,溶液的总体积为20mL 在B.点所示的溶液中,阳离子浓度最大的是Na 在A.点所示的溶液中:
当溶液pH为7时,溶液的总体积为20mL 在B.点所示的溶液中,阳离子浓度最大的是Na 在A.点所示的溶液中:
 H++A2- 当V(NaOH)=20mL时,则有:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(0H-)
H++A2- 当V(NaOH)=20mL时,则有:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(0H-) 
