你可能感兴趣的试题
构成原电池正极和负极的材料必须是两种金属 由铜、锌电极与硫酸铜溶液组成的原电池铜是负极 电子沿导线由锌流向铜,通过硫酸溶液被氢离子得到而放出氢气 铜锌原电池工作时,锌与硫酸反应,所以才产生电子
构成原电池正极和负极的材料必须是两种金属 由铜锌作为电极与硫酸铜溶液组成的原电池中,铜是负极 电流通过硫酸溶液,SO42- 向正极移动 铜锌原电池工作时,若有13 g锌被溶解,电路中就有0.4 mol 电子通过
锌片为负极,且逐渐溶解 铜片为正极,铜不易失电子而受到保护 电子由锌片通过导线流向铜片,H+往铜片运动 该装置能将电能转变为化学能
手机上用的锂离子电池属于二次电池 铜锌原电池工作时,电子沿外电路从铜电极流向锌电极 甲醇燃料电池可把化学能转化为电能 锌锰干电池中,锌电极是负极
在镁、铝、稀NaOH溶液组成的原电池中,镁是负极,铝是正极 在铁、铝、稀硫酸组成的原电池中,电子由铁片通过导线流向铝片 在锌、铜、稀硫酸组成的原电池中,当电池工作时,硫酸根离子向正极移动 在锌、铜、CuSO4溶液组成的原电池中,负极质量减轻,正极质量增加
锌片为负极,且锌片逐渐溶解 铜为正极,铜不易失电子而受到保护 电子由铜片通过导线流向锌片 该装置能将化学能转变为电能 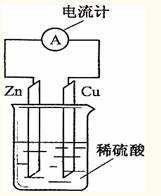
电子由铜片通过导线流向锌片 锌得电子,被还原 锌为负极,铜为正极 该装置能将电能转变为化学能
构成原电池正极和负极的材料必须是两种金属 由铜、锌电极与硫酸铜溶液组成的原电池铜是负极 电子沿导线由锌流向铜,通过硫酸溶液被氢离子得到而放出氢气 铜锌原电池工作时,锌被硫酸溶解,所以才产生电子
构成原电池正极和负极的材料必须是两种金属 由铜、锌作电极与硫酸铜溶液组成的原电池中铜是负极 电子沿外导线由锌流向铜,通过硫酸溶液被氢离子得到而放出氢气 铜锌原电池工作时,若有13 g锌被溶解,电路中就有0.4 mol电子通过
构成原电池正极和负极的材料必须是两种金属 在该原电池中,铜作负极 铜锌原电池工作时,若有13g锌溶解,则电路中就有0.4moI电子通过 电子通过硫酸溶液由锌流向铜,在铜电极上被氢离子得到而放出氢气
正极和负极必须是两种不同的金属 原电池工作时,正极和负极上发生的都是氧化还原反应 原电池是把化学能转化成电能的装置 锌、铜和盐酸构成的原电池工作时,锌片上有6.5g锌溶解,正极上就有0.1g氢气生成
铜在原电池中作负极,在电镀池中作阳极 原电池溶液增加的质量比电镀池阴极增加的质量大 锌棒每减少0.65 g,导线上转移的电子就为0.02 mol 电镀池中的电解质溶液可用ZnSO4溶液
该原电池中,铜为正极 该原电池中,电子由铜片经过导线流入锌片 该原电池工作一段时间后,溶液的酸性减弱 该原电池工作一段时间后,锌片质量减小
锌片逐渐溶解 烧杯中溶液逐渐呈蓝色 电子由铜片通过导线流向锌片 该装置能将电能转变为化学能
构成原电池正极和负极的材料必须是两种金属 由铜、铁作电极与浓硝酸组成的原电池中铜是负极 电子沿外导线由锌流向铜,通过硫酸溶液被氢离子得到而放出氢气 铜锌原电池工作时,若有13克锌被溶解,电路中就有0.4mol电子通过
原电池是将化学能转化为电能的装置 在原电池中,电子流出的一极是负极,发生氧化反应 锌、铜、硫酸组成的原电池中,溶液中的 Zn2+、 H+均向正极移动 构成原电池的两个电极必须是活泼性不同的两种金属
构成原电池正极和负极的材料必须是两种金属 由铜、锌作电极与硫酸铜溶液组成的原电池中铜是负极 马口铁(镀锡铁)破损时与电解质溶液接触,锡先被腐蚀 铜锌原电池工作时,若有13g锌被溶解,电路中就有0.4mol电子通过
锌片为负极,且锌片逐渐溶解 铜片为正极,且铜片上有气泡 电子由铜片通过导线流向锌片 该装置能将化学能转变为电能 
原电池是把电能转化为化学能的装置 原电池中电子流入的一极是正极,发生还原反应 铜锌原电池中电子由锌电极经过溶液到铜电极 原电池中的阳离子向负极移动
在镁、铝、稀NaOH溶液组成的原电池中,镁是负极,铝是正极 在铁、铝、稀硫酸组成的原电池中,电子由铁片通过导线流向铝片 在锌、铜、稀硫酸组成的原电池中,当电池工作时,硫酸根离子向正极移动 在锌、铜、CuSO4溶液组成的原电池中,负极质量减轻,正极质量增加


