你可能感兴趣的试题
容器①、②中反应的平衡常数相等 平衡时,两个容器中NH3的体积分数相等 若容器①的体积为0.5L.,则平衡时放出的热量小于23.15 kJ 容器②中达平衡时放出的热量Q.=23.15 kJ
B.C.内分别充入等质量的X.、H2、Y.三种气体,当隔板静止时,A.C.内的气体密度相等。下列说法不正确的是  A.摩尔质量: M(X)=M(Y) 分子数目:N(X)=N(Y) 气体的体积:V(X)=V(Y) 物质的量: n(X)
A.摩尔质量: M(X)=M(Y) 分子数目:N(X)=N(Y) 气体的体积:V(X)=V(Y) 物质的量: n(X)
容器①、②中反应的平衡常数相等 平衡时,两个容器中NH3的体积分数均为 容器②中达平衡时放出的热量Q.=23.15 kJ 若容器①的体积为0.5L.,则平衡时放出的热量小于23.15 kJ
容器②中达平衡时放出的热量Q.=23.15 kJ 若容器①的体积为0.5L.,则平衡时放出的热量小于23.15 kJ
容器①、②中反应的平衡常数相等 平衡时,两个容器中NH3的体积分数相等 若容器①的体积为0.5L.,则平衡时放出的热量小于23.15 kJ 容器②中达平衡时放出的热量Q.=23.15 kJ
容器②中达平衡时放出的热量Q=23. 15kJ 平衡时,两个容器中NH3的体积分数均为1/7 容器①、②中反应的平衡常数相等 若容器①体积为0. 5L,则平衡时放出的热量小于23. 15kJ
容器①、②中反应的平衡常数相等 平衡时,两个容器中NH3的体积分数均为 容器②中达平衡时放出的热量Q.=23.15 kJ 若容器①的体积为0.5 L,则平衡时放出的热量小于23.15 kJ
容器②中达平衡时放出的热量Q.=23.15 kJ 若容器①的体积为0.5 L,则平衡时放出的热量小于23.15 kJ
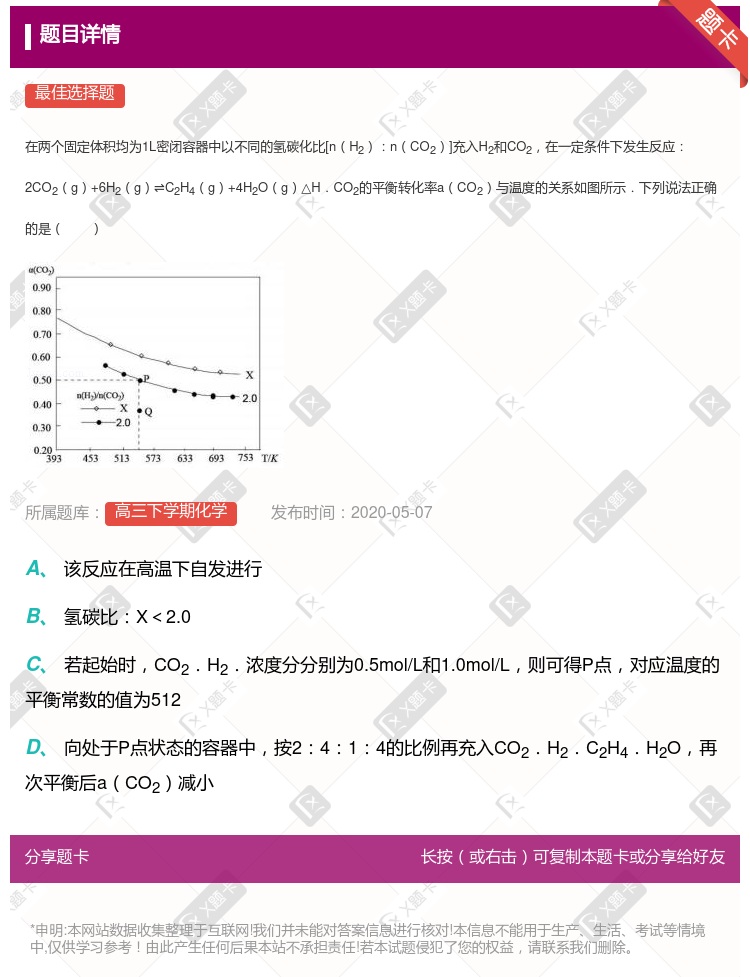
该反应在高温下自发进行 氢碳比:X<2.0 氢碳比为2.0时.Q.点v(H2)逆小于P.点的v(H2)逆 向处于P.点状态的容器中,按2:4:1:4的比例再充入 C.02、H2、C2H4. H20,再次平衡后a(C.02)减小
容器①、②中反应的平衡常数相等 平衡时,两个容器中NH3的体积分数相等 若容器①的体积为0.5L.,则平衡时放出的热量小于23.15 kJ 容器②中达平衡时放出的热量Q.=23.15 kJ
2molB和1molA.1mol 相同条件下发生如下反应:A.(g)+B(g)  xC(g) △H<0.测得两容器中cA.随时间t的变化如图所示。下列说法错误的是: A.x可能等于2也可能等于3 B.若向平衡后的乙容器充入 ,则再次达到平衡时A.的体积分数减小 C.若升高甲容器的温度,可使甲容器中各物质的体积分数与乙容器相同 若其它条件不变,使乙容器体积变为2L,则平衡时乙容器中:0.25mol/L
xC(g) △H<0.测得两容器中cA.随时间t的变化如图所示。下列说法错误的是: A.x可能等于2也可能等于3 B.若向平衡后的乙容器充入 ,则再次达到平衡时A.的体积分数减小 C.若升高甲容器的温度,可使甲容器中各物质的体积分数与乙容器相同 若其它条件不变,使乙容器体积变为2L,则平衡时乙容器中:0.25mol/L
2molB和1molA.1mol 相同条件下发生如下反应:A.(g)+B(g)  xC(g) △H<0.测得两容器中cA.随时间t的变化如图所示。下列说法错误的是: A.x可能等于2也可能等于3 B.若向平衡后的乙容器充入 ,则再次达到平衡时A.的体积分数减小 C.若升高甲容器的温度,可使甲容器中各物质的体积分数与乙容器相同 若其它条件不变,使乙容器体积变为2L,则平衡时乙容器中:0.25mol/L
xC(g) △H<0.测得两容器中cA.随时间t的变化如图所示。下列说法错误的是: A.x可能等于2也可能等于3 B.若向平衡后的乙容器充入 ,则再次达到平衡时A.的体积分数减小 C.若升高甲容器的温度,可使甲容器中各物质的体积分数与乙容器相同 若其它条件不变,使乙容器体积变为2L,则平衡时乙容器中:0.25mol/L
容器①、②中反应的平衡常数相等 平衡时,两个容器中NH3的体积分数均为 容器②中达平衡时放出的热量Q.=23.15 kJ 若容器①的体积为0.5L.,则平衡时放出的热量小于23.15 kJ
容器②中达平衡时放出的热量Q.=23.15 kJ 若容器①的体积为0.5L.,则平衡时放出的热量小于23.15 kJ
容器①、②中反应的平衡常数相等 平衡时,两个容器中NH3的体积分数均为1/7 容器②中达平衡时放出的热量Q.=23.15 kJ 若容器①体积为0.5L,则平衡时放出的热量<23.15kJ
该反应在高温下自发进行 氢碳比:X<2.0 氢碳比为2.0时,Q.点v(H2)逆小于P.点的v(H2)逆 向处于P.点状态的容器中,按2∶4∶1∶4的比例再充入CO2、H2、C2H4、H2O,再次平衡后a(CO2)减小
容器②中达平衡时放出的热量Q.=23.15 kJ 平衡时,两个容器中NH3的体积分数均为 容器①、②中反应的平衡常数相等 若容器①体积为0.5L,则平衡时放出的热量<23.15kJ
容器①、②中反应的平衡常数相等 若容器①体积为0.5L,则平衡时放出的热量<23.15kJ
容器②中达平衡时放出的热量Q=23. 15kJ 平衡时,两个容器中NH3的体积分数均为1/7 容器①、②中反应的平衡常数相等 若容器①体积为0. 5L,则平衡时放出的热量小于23. 15kJ
若容器甲体积为0.5L.,则平衡时放出的热量小于23.15 kJ 容器乙中达平衡时放出的热量Q.=23.15 kJ 容器甲、乙中反应的平衡常数相等 平衡时,两个容器中XY3的体积分数均为1/7
容器①、②中反应的平衡常数相等 容器②中反应达到平衡时放出的热量为23.15 kJ 达平衡时,两个容器中XY3的物质的量浓度均为2 mol·L-1 若容器①体积为0.20L.,则达平衡时放出的热量大于23.15 kJ
 A.摩尔质量: M(X)=M(Y) 分子数目:N(X)=N(Y) 气体的体积:V(X)=V(Y) 物质的量: n(X)
A.摩尔质量: M(X)=M(Y) 分子数目:N(X)=N(Y) 气体的体积:V(X)=V(Y) 物质的量: n(X) 容器②中达平衡时放出的热量Q.=23.15 kJ 若容器①的体积为0.5L.,则平衡时放出的热量小于23.15 kJ
容器②中达平衡时放出的热量Q.=23.15 kJ 若容器①的体积为0.5L.,则平衡时放出的热量小于23.15 kJ
 容器②中达平衡时放出的热量Q.=23.15 kJ 若容器①的体积为0.5 L,则平衡时放出的热量小于23.15 kJ
容器②中达平衡时放出的热量Q.=23.15 kJ 若容器①的体积为0.5 L,则平衡时放出的热量小于23.15 kJ
 xC(g) △H<0.测得两容器中cA.随时间t的变化如图所示。下列说法错误的是: A.x可能等于2也可能等于3 B.若向平衡后的乙容器充入 ,则再次达到平衡时A.的体积分数减小 C.若升高甲容器的温度,可使甲容器中各物质的体积分数与乙容器相同 若其它条件不变,使乙容器体积变为2L,则平衡时乙容器中:0.25mol/L
xC(g) △H<0.测得两容器中cA.随时间t的变化如图所示。下列说法错误的是: A.x可能等于2也可能等于3 B.若向平衡后的乙容器充入 ,则再次达到平衡时A.的体积分数减小 C.若升高甲容器的温度,可使甲容器中各物质的体积分数与乙容器相同 若其它条件不变,使乙容器体积变为2L,则平衡时乙容器中:0.25mol/L xC(g) △H<0.测得两容器中cA.随时间t的变化如图所示。下列说法错误的是: A.x可能等于2也可能等于3 B.若向平衡后的乙容器充入 ,则再次达到平衡时A.的体积分数减小 C.若升高甲容器的温度,可使甲容器中各物质的体积分数与乙容器相同 若其它条件不变,使乙容器体积变为2L,则平衡时乙容器中:0.25mol/L
xC(g) △H<0.测得两容器中cA.随时间t的变化如图所示。下列说法错误的是: A.x可能等于2也可能等于3 B.若向平衡后的乙容器充入 ,则再次达到平衡时A.的体积分数减小 C.若升高甲容器的温度,可使甲容器中各物质的体积分数与乙容器相同 若其它条件不变,使乙容器体积变为2L,则平衡时乙容器中:0.25mol/L 容器②中达平衡时放出的热量Q.=23.15 kJ 若容器①的体积为0.5L.,则平衡时放出的热量小于23.15 kJ
容器②中达平衡时放出的热量Q.=23.15 kJ 若容器①的体积为0.5L.,则平衡时放出的热量小于23.15 kJ
 容器①、②中反应的平衡常数相等 若容器①体积为0.5L,则平衡时放出的热量<23.15kJ
容器①、②中反应的平衡常数相等 若容器①体积为0.5L,则平衡时放出的热量<23.15kJ