你可能感兴趣的试题
2[N]=(N2) 1/2N2=[N] [N]=(N) 以上都不是
原子核外每一能层最多可容纳的电子数2n2(n为能层序数) 能层序数越大,s原子轨道的半径越大 各能级包含的原子轨道数按s、p、d、f的顺序依次为1、3、5、7 1个原子轨道里最多只能容纳2个电子,且自旋方向相同
原子核外的电子云是分层排布的,电子壳层可用主量子数表示 主量子数为n的壳层(非最外层)可容纳的电子数为2n2一1 愈外面的壳层可容纳的电子数愈多(非最外层) 最外层电子数最多不超过8个 同一电子壳层中电子具有的能量及运动形式不同
O2- — 氧离子 3H — 3个氢元素 Fe3O.4 — 四氧化三铁 2N2 — 2个氮气分子
加催化剂同时升高温度 加催化剂同时增大压强 升高温度同时充入N2 降低温度同时增大压强
原子处于最低能量状态(最稳定)叫基态 电子在各个轨道上的能量连续分布 电子从低能级过渡到某一高能级上称原子的激发 电子能级跃迁产生特征X线 跃迁产生光子的能量等于两能级结合能之差
两个氮气分子:2N2 淀粉的化学式:(C6 H10O6)n 臭氧中氧元素的化合价: 一氧化碳使氧化铜还原成铜的化学方程式:
一氧化碳使氧化铜还原成铜的化学方程式:
核外的带负电荷的电子称为“电子云” 物质由原子组成 一般每层上的电子数最多是2n2个 核外电子具有不同壳层 最外层电子数最多不超过10个
CH4 (g)+2NO2 (g)= N2 (g)+CO2 (g)+2H2O (l) △H.=-867 kJ·mol-1 若0.2 mol CH4还原NO2至N2,在上述条件下放出的热量为173.4 kJ 1molCH4催化还原NOx为N2的过程中,若x=1.6,则转移的电子为3.2 mol 若用4.48L CH4还原NO2至N2,整个过程中转移的电子为3.2 mol
原子由核及电子组成 核外电子具有不同壳层 壳层中都含有一定数目的电子轨迹 半径最小的壳层叫L层 一般每层上的电子数最多是2n2个
K层最多只能容纳2个电子 M层最多时可容纳32个电子 最外层的电子束≥8 越外面的壳层可容纳的电子束越少 L层能容纳6个电子
物质由原子组成 核外电子具有不同壳层 每一壳层上可容纳的电子数最多是2n2个 核外的带负电荷的电子称为“电子云” 原子最外层上的电子数一般不超过18个
2n2e 2n2e+(1/2)λ 2n2e+λ 2n2e+λ/2n2

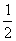 ) (-1, -1) (
) (-1, -1) ( ) (
) ( , -1)
, -1)
 一氧化碳使氧化铜还原成铜的化学方程式:
一氧化碳使氧化铜还原成铜的化学方程式: