你可能感兴趣的试题
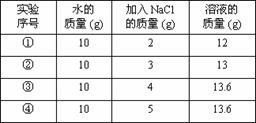
②中所得溶液是饱和溶液 20℃时10g水最多能溶解4g NaCl ③④溶液的溶质质量分数相等 ①所得溶液的溶质质量分数为20%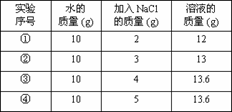
②中所得溶液是饱和溶液 20℃时10g水最多能溶解4gNaCl ③④溶液的溶质质量分数相等 ①所得溶液的溶质质量分数为20%
②中所得溶液是饱和溶液 20℃时10g水最多能溶解4g NaCl ③④溶液的溶质质量分数相等 ①所得溶液的溶质质量分数为20%
m(溶质):m(溶剂)=20:100 此时溶液中溶质的质量分数为20% 再加入少量NaCl固体,溶质的质量分数变大 蒸发溶剂析出晶体后,溶液变成不饱和溶液
用50g溶质质量分数为10%的NaCl溶液配制溶质质量分数为5%的NaCl溶液需要加水20g 气体的溶解度与温度、压强和水的用量有关 饱和溶液一定是浓溶液,不饱和溶液一定是稀溶液 汽油作溶剂可以去除衣物上的油污
②中所得溶液是饱和溶液 20℃时10g水最多能溶解4g NaCl ③④溶液的溶质质量分数相等 ①所得溶液的溶质质量分数为20%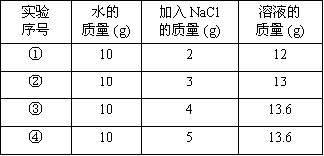
饱和溶液不一定是浓溶液 饱和溶液是不能再溶解任何其他物质的溶液 溶质的质量分数为20%的KNO3溶液100 g取出50 g,则剩余溶液中溶质的质量分数为10% NaCl的溶解度是36 g,是指在100 g水中最多可溶解36 g NaCl
②中所得溶液是饱和溶液 20℃时10g水最多能溶解4gNaCl ③④溶液的溶质质量分数相等 ①所得溶液的溶质质量分数为20% 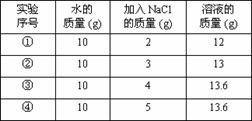
②中所得溶液是饱和溶液 20℃时10g水最多能溶解4g NaCl ③④溶液的溶质质量分数相等 ①所得溶液的溶质质量分数为20%
该温度下NaCl的溶解度S.= g 溶液中溶质的物质的量浓度c(NaCl) = mol·L-1 溶液中溶质的物质的量浓度c(NaCl) = mol·L-1 溶液中溶质的质量分数w=%
在该溶液中,溶质和溶剂的质量比为1:5 100克水中含有20克NaCl 在该溶液中,溶质与溶液的质量比为1:6 50克该溶液中含有NaCl为10克
NaCl的溶解度大于KNO3的溶解度 t1℃时,KNO3饱和溶液中溶质的质量分数是20% 在温度高于t2℃时,100gKNO3饱和溶液中溶质的质量 大于100g NaCl饱和溶液中溶质的质量 t2℃时的NaCl溶液与KNO3溶液中,溶质的质量分数相等
100g水中溶解了20g蔗糖 100g蔗糖溶液中溶解了20 g蔗糖 溶液中的溶质是蔗糖,溶剂是水 从20%的蔗糖溶液中取出一滴,这滴溶液中溶质的质量分数仍是20%
②中所得溶液是饱和溶液 20℃时10g水最多能溶解4g NaCl ③④溶液的溶质质量分数相等 ①所得溶液的溶质质量分数为20% 
②中所得溶液是饱和溶液 20℃时10g水最多能溶解4g NaCl ③④溶液的溶质质量分数相等 ①所得溶液的溶质质量分数为20%
①②所待溶液是20℃时NaCl的不饱和溶液 ①②③所得溶液是20℃时NaCl的不饱和溶液 20℃时NaCl的溶解度为3.6g ①所得溶液的溶质的质量分数为20g
加入10 gNaCl 加入水5 g 蒸发掉50 g水 加入100 g溶质质量分数为10%的NaCl溶液