你可能感兴趣的试题
a点正反应速率大于逆反应速率 增大X.的浓度,X.的转化率增大 容器中压强恒定时,不能说明反应已达平衡状态 保持温度和密闭容器的容积不变,再充入1 molX.和2 molY.,再次达到平衡时n(Z)/n(X)的值会变小
向一定量的水中加入生石灰 红磷在装有空气的密闭容器中燃烧 向一定量的烧碱溶液中加入盐酸 向饱和KNO3溶液中加入KMnO4固体
v正(NH3)=2v逆(CO2) 密闭容器中总压强不变 密闭容器中混合气体的密度不变 密闭容器中氨气的体积分数不变
①水的电解 ②木炭在密闭的容器内燃烧 ③加热一定量的高锰酸钾制氧气 ④20℃时,向一定量接近饱和的硝酸钾溶液中加入硝酸钾固体
密闭容器中气体的平均相对分子质量不变则该反应达到平衡状态 该反应在任何条件下都能自发进行 再加入一定量氨基甲酸铵,可加快反应速率 保持温度不变,压缩体积,达到新的平衡时,NH3的浓度不变
向一定量的稀盐酸和CaCl2混合溶液中滴入Na2CO3 溶液 向一定量的MnO2固体中加入一定量的过氧化氢溶液 向一定量的稀盐酸中滴入NaOH溶液 向一定温度时一定量的饱和石灰水中加入生石灰
从反应开始到平衡,用O2表示的平均反应速率为0.05mol/(L·min) 达到平衡状态时,SO2的转化率为80% 该温度下反应的平衡常数约为20.83 保持容器容积不变,再充入0.5molSO2,平衡正向移动,平衡常数增大
若缩小容器的体积,则容器中气体的颜色先变深后又变浅 若压强不变,向容器中再加入一定量的N2O4,再次达到平衡时各种物质的百分含量不变 若体积不变,向容器中再加入一定量的N2O4,平衡向逆反应方向移动,再次平衡时N2O4的转化率将降低 若体积不变,升高温度,再次平衡时NO2的浓度将增大
向一定量的MnO2中加入H2O2溶液 向生铁中加稀盐酸 红磷在盛有空气的密闭容器中燃烧 加热一定量的高锰酸钾固体
某温度下,向一定量接近饱和的硝酸钾溶液中不断加入硝酸钾晶体 向一定量的氢氧化钠溶液中滴加过量的氯化铁溶液 向稀盐酸中滴加过量的烧碱溶液 镁在密闭容器(含有空气)内燃烧,容器内元素的种类随时间的变化情况 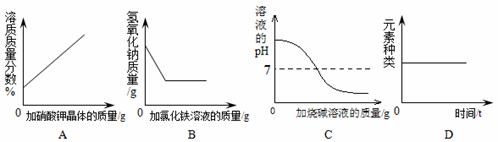
和6mol ,发生如下反应:2A(g)+3B(g) 4C(g)+D(g)反应10min后达平衡,此时D.的浓度为0.5mol/L。下列说法正确的是( ) A.前10min反应的平均速率V.( )=0.10mol/L·min B.反应达平衡时B.的平衡浓度是1.5mol/L C.恒温下将反应容器体积缩小一半,则 的平衡浓度小于1.0mol/L D.10min后向容器中加入A.,重新平衡时A.的转化率一定大于50%
4C(g)+D(g)反应10min后达平衡,此时D.的浓度为0.5mol/L。下列说法正确的是( ) A.前10min反应的平均速率V.( )=0.10mol/L·min B.反应达平衡时B.的平衡浓度是1.5mol/L C.恒温下将反应容器体积缩小一半,则 的平衡浓度小于1.0mol/L D.10min后向容器中加入A.,重新平衡时A.的转化率一定大于50%
水的电解 木炭在密闭的容器内燃烧 加热一定量的高锰酸钾制氧气 20 ℃时,向一定量接近饱和的硝酸钾溶液中加入硝酸钾固体
在密闭容器中燃烧一定量的红磷 加热一定量的高锰酸钾固体 在少量二氧化锰中加入双氧水 加热一定量的氯酸钾和二氧化锰的混合物
密闭容器中气体的平均相对分子质量不变则该反应达到平衡状态 20℃时氨基甲酸铵的分解平衡常数为2.048×10-9mol3·L-3 恒温下压缩体积,NH3的体积分数不变 再加入一定量氨基甲酸铵,可加快正反应反应速率
a点正反应速率大于逆反应速率 增大X.的浓度,X.的转化率增大 容器中压强恒定时,不能说明反应已达平衡状态 保持温度和密闭容器的压强不变,再充入1 molX.和 2 molY.,再次达到平衡时n(Z)/n(X)的值会变小
增大X.的浓度,X.的转化率增大 容器中压强恒定时,不能说明反应已达平衡状态 保持温度和密闭容器的压强不变,再充入1 molX.和 2 molY.,再次达到平衡时n(Z)/n(X)的值会变小
某温度下,向一定量接近饱和的硝酸钾溶液中不断加入硝酸钾晶体 向一定量的氢氧化钠溶液中滴加过量的氯化铁溶液 向稀盐酸中滴加过量的烧碱溶液 镁在密闭容器(含有空气)内燃烧,容器内元素的种类随时间的变化情况


 4C(g)+D(g)反应10min后达平衡,此时D.的浓度为0.5mol/L。下列说法正确的是( ) A.前10min反应的平均速率V.( )=0.10mol/L·min B.反应达平衡时B.的平衡浓度是1.5mol/L C.恒温下将反应容器体积缩小一半,则 的平衡浓度小于1.0mol/L D.10min后向容器中加入A.,重新平衡时A.的转化率一定大于50%
4C(g)+D(g)反应10min后达平衡,此时D.的浓度为0.5mol/L。下列说法正确的是( ) A.前10min反应的平均速率V.( )=0.10mol/L·min B.反应达平衡时B.的平衡浓度是1.5mol/L C.恒温下将反应容器体积缩小一半,则 的平衡浓度小于1.0mol/L D.10min后向容器中加入A.,重新平衡时A.的转化率一定大于50%
 增大X.的浓度,X.的转化率增大 容器中压强恒定时,不能说明反应已达平衡状态 保持温度和密闭容器的压强不变,再充入1 molX.和 2 molY.,再次达到平衡时n(Z)/n(X)的值会变小
增大X.的浓度,X.的转化率增大 容器中压强恒定时,不能说明反应已达平衡状态 保持温度和密闭容器的压强不变,再充入1 molX.和 2 molY.,再次达到平衡时n(Z)/n(X)的值会变小