你可能感兴趣的试题
和3 mol 在一定条件下反应:A.(g)+xB.(g)  2C(g), 2 min后达到平衡,生成0.4 mol ,测得混合气体共3.4 mol,则下列结果正确的是 A.平衡时,物质的量之比nA.∶nB.∶nC.=2∶11∶4 B.x值等于3 C.A.的转化率为20% B.的平均反应速率为0.4 mol/(L·min)
2C(g), 2 min后达到平衡,生成0.4 mol ,测得混合气体共3.4 mol,则下列结果正确的是 A.平衡时,物质的量之比nA.∶nB.∶nC.=2∶11∶4 B.x值等于3 C.A.的转化率为20% B.的平均反应速率为0.4 mol/(L·min)
放电时电池正极为NaxCn 放电时Na+向电极Ⅱ移动 充电时阳极反应:NaxCn-xe-=nC+xNa+ 充电时电极Ⅰ与外电源正极相连
F.Na=F.Nb=F.Nc F.Na>F.Nb>F.Nc F.NaF.Na>F.Nb=F.Nc
放电时电池正极为NaxCn 放电时Na+向电极Ⅱ移动 充电时阳极反应:NaxCn-xe-=nC+xNa+ 充电时电极Ⅰ与外电源正极相连
Na<G Nb<G Nc<G Nd<G. 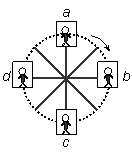
FNa=FNb=FNc FNb>FNa>FNc FNbNaNc FNa>FNb=FNc
①和②产物的阴阳离子个数比不相等 ①和②生成等物质的量的产物,转移电子数不同 常温下Na与足量O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快 25℃、101kPa下:Na2O2(s)+2Na(s)=2Na2O(s) △H= -317kJ mol-1
mol-1
①和②产物的阴阳离子个数比不相等 ①和②生成等物质的量的产物,转移电子数不同 常温下Na与足量O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快 25℃101kPa下,Na2O2(s)+2Na(s)═2Na2O(s)△H=﹣317kJ/mol
ωna=ωnb,ωna≠ωnc ωna=ωnb=ωnc ωna=ωnc,ωna≠ωnb ωnc=ωnb,ωna≠ωnb
n(Na7C03)=n(1/2Na2CO3) n(Na2C03)=2n(1/2Na2CO3) 2n(Na2CO3)=n(1/2Na2C03) 不确定
反应①和②均属于放热反应 ①和②产物的阴阳离子个数比相同 ①和②生成等物质的量的产物,转移电子数不同 反应Na2O2(s)+2Na(s)=2 Na2O(s)的△H =- 317 kJ/mol

 2C(g), 2 min后达到平衡,生成0.4 mol ,测得混合气体共3.4 mol,则下列结果正确的是 A.平衡时,物质的量之比nA.∶nB.∶nC.=2∶11∶4 B.x值等于3 C.A.的转化率为20% B.的平均反应速率为0.4 mol/(L·min)
2C(g), 2 min后达到平衡,生成0.4 mol ,测得混合气体共3.4 mol,则下列结果正确的是 A.平衡时,物质的量之比nA.∶nB.∶nC.=2∶11∶4 B.x值等于3 C.A.的转化率为20% B.的平均反应速率为0.4 mol/(L·min)
 ,na>nb
,na>nb  ,na
,na ,na
,na ,na>nb
,na>nb 

 mol-1
mol-1