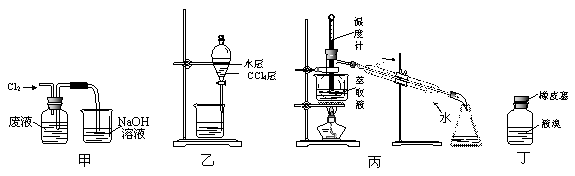你可能感兴趣的试题
装置①和装置③中都盛有水,其作用相同 装置②和装置④中都盛有NaOH溶液,其吸收的杂质相同 产物可用分液的方法进行分离,1,2﹣二溴乙烷应从分液漏斗的上口倒出 制备乙烯和生成1,2﹣二溴乙烷的反应类型分别是消去反应和加成反应
用装置甲氧化废液中的溴化氢 用装置乙分离CCl4层和水层 用装置丙分离CCl4和液溴 用仪器丁长期贮存液溴
用装置甲氧化废液中的溴化氢 用装置乙分离CCl4层和水层 用装置丙分离CCl4和液溴 用仪器丁长期贮存液溴
少量液溴可用水封存,减少溴挥发 浓硝酸用带橡胶塞的细口、棕色试剂瓶盛放 实验室可以用浓氨水和生石灰制备NH3 实验室中用加热方法分离碘和食盐的混合物
图1——测量锌与硫酸反应的速率 图2——灼烧海带成海带灰 图3——验证溴乙烷与NaOH乙醇溶液反应生成乙烯 图4——实验室制备收集乙酸乙酯
实验室用图1所示装置萃取、分离溴水中的溴 用铜丝蘸取草木灰在酒精灯火焰上灼烧检验钾元素 实验室用图2所示装置制备少量乙酸乙酯 用精度为0.001 g的电子天平称量5.850 g氯化钠,将其溶解、洗涤后,将溶液全部转移到100 mL的容量瓶中,定容配成1.00 mol·L-1氯化钠溶液
①装置用于检验1-溴丙烷消去产物 ②装置用于石油的分馏  ③装置用于实验室制硝基苯 ④装置可装置证明酸性:盐酸>碳酸>苯酚
③装置用于实验室制硝基苯 ④装置可装置证明酸性:盐酸>碳酸>苯酚
图1为实验室制备硝基苯的装置 图2中振荡后下层为无色 用图3所示的实验装置制备乙酸乙酯 图4装置可以达到验证溴乙烷发生消去反应生成烯烃的目的
图1——测量锌与硫酸反应的速率 图2——灼烧海带成海带灰 图3——验证溴乙烷与NJaOH乙醇溶液反应生成乙烯 图4——实验室制备收集乙酸乙酯
用装置甲制取氯气 用装置乙使Br-全部转化为溴单质 用装置丙分液时先从下口放出水层,再从上口倒出有机层 用装置丁将分液后的水层蒸发至干,再灼烧制得无水FeCl3
用装置甲氧化废液中的溴化氢 用装置乙分离CCl4层和水层 用装置丙分离CCl4和液溴 用仪器丁长期贮存液溴 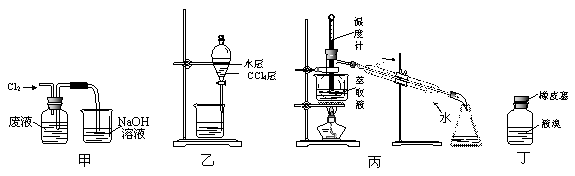
配制0.1 mol·L-1烧碱溶液时,容量瓶应用0.1 mol·L-1 烧碱溶液润洗 在蒸发溶液时,不能将溶液直接蒸干 实验室可用图 1 所示装置制备乙酸丁酯(已知反应温度为 115~125℃) 实验室用图2 所示装置制备氢气时,该装置符合“随开随 制,随关随停”的要求
实验室用液溴、苯和铁制备溴苯时必须加热 实验室可用如下图所示装置进行酯化实验 如果甲烷中混有少量乙烯,可以通过盛有酸性KMnO4溶液进行除杂 将加热后的铜丝多次插入乙醇中,乙醇中可以闻到刺激性气味
实验室用图1装置制备Cl2 加热后图2中溶液颜色恢复红色 用图3装置配制150 mL稀盐酸 实验室用图4装置制取少量蒸馏水
喷泉实验 实验室制取并收集氨气 制备氢氧化亚铁 验证苯中是否有碳碳双键


 ③装置用于实验室制硝基苯 ④装置可装置证明酸性:盐酸>碳酸>苯酚
③装置用于实验室制硝基苯 ④装置可装置证明酸性:盐酸>碳酸>苯酚