你可能感兴趣的试题
电流从右侧电极经过负载后流向左侧电极 为使电池持续放电,离子交换膜需选用阴离子交换膜 电极A.极反应式为2NH3-6e-=N2+6H+ 当有4.48LNO2(标准状况) 被处理时,转移电子为0.8mol 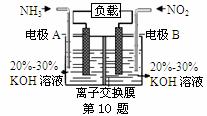
NO2为酸性氧化物 H2O很稳定是因为水分子之间存在氢键 反应③中每生成22.4 LN2,转移电子数1.5NA NH3的沸点比PH3的沸点高
该装置是将电能转化为化学能 OH−通过阴离子交换膜向电极甲迁移 电极乙的电极反应式为2NO2+8e−+8H+== N2↑+4H2O 当电路中通过2mol电子时,有11.2 LNO2 被完全处理
CH4+2O2→CO2+2H2O HCl+NaOH=NaCl+H2O Mg3N2+6H2O=3Mg(OH)2↓+2NH3↑ Ba(OH)2·8H2O+2NH4Cl=BaCl2+2NH3·H2O+8H2O
2NH3 + 3CuO → 3Cu + N2 +3H2O 2Na + 2NH3 → 2NaNH2 + H2↑ 4NH3 + 6NO → 5N2 + 6H2O 3SiH4 + 4NH3 → Si3N4 + 12H2
H2O (l)+CaO(s) =Ca(OH)2(s) Ba(OH)2·8H2O+2NH4Cl=BaCl2+2NH3·H2O+8H2O 2KClO3 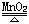 2KCl+3O2↑ CH4(g)+2O2(g)=CO2(g)+2H2O(l)
2KCl+3O2↑ CH4(g)+2O2(g)=CO2(g)+2H2O(l)
NH3 + H2O = NH3·H2O 3Cl2 + 8NH3 = N2 + 6NH4Cl
3CuO + 2NH3 3Cu + N2 + 3H2O NH3 + HNO3 = NH4NO3
2Na + 2NH3 → 2NaNH2 + H2↑ 2NH3 + 3CuO → 3Cu + N2 +3H2O NH3+HCl=NH4Cl 3SiH4 + 4NH3 → Si3N4 + 12H2
电流从左侧电极经过负载后流向右侧电极 为使电池持续放电,离子交换膜需选用阴离子交换膜 电极A极反应式为2NH3-6e-===N2+6H+ 当有4.48 L NO2被处理时,转移电子数为0.8N.A
NO+NO2+2NH3→2N2+3H2O 4NO+4NH3+O2→4N2+6H2O 6NO2+8NH3→7N2+12H2O A+C
2 NH3 +2Na==2NaNH2 +H2 8 NH3+3 Cl2==6NH4Cl+N2 2 NH3+3CuO==N2+3Cu+3H2O 4 NH3+6NO==5N2+6H2O
2 NH3 +2Na==2NaNH2 +H2 8 NH3+3 Cl2==6NH4Cl+N2 2 NH3+3CuO==N2+3Cu+3H2O 4 NH3+6NO==5N2+6H2O
4NH3+3O2===2N2+6H2O 2NO===N2+O2 4NH3+5O2===4NO+6H2O 4NH3+6O2===5N2+6H2O
4NH3+3O2===2N2+6H2O 2NO===N2+O2 4NH3+5O2===4NO+6H2O 4NH3+6NO===5N2+6H2O
2Na + 2NH3 → 2NaNH2 + H2↑ NH3 + HNO3→ NH4NO3 4NH3 + 6NO → 5N2 + 6H2O 3SiH4 + 4NH3 → Si3N4 + 12H2
:燃料电池正极充入N2 :电池的负极反应为H2-2e-=2H+ :电池的正极反应为 N2+6e-+6H+==2NH3 :电池工作时正极发生还原反应
5v(NH3)/6=v(O2) 5v(O2)/6=v(H2O)
2v(NH3)/2=v(H2O) 4v(O2)/5=v(NO)
2Na+2NH3===2NaNH2+H2↑ NH3+HCl===NH4Cl 4NH3+6NO===5N2+6H2O 3SiH4+4NH3===Si3N4+12H2


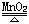 2KCl+3O2↑ CH4(g)+2O2(g)=CO2(g)+2H2O(l)
2KCl+3O2↑ CH4(g)+2O2(g)=CO2(g)+2H2O(l)