
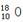 氯原子的结构示意图:
氯原子的结构示意图: Fe3+的最外层电子排布式为3s23p63d5 基态铜原子的外围电子排布图:
Fe3+的最外层电子排布式为3s23p63d5 基态铜原子的外围电子排布图:
 因氧元素电负性比氮元素大,故氧原子第一电离能比氮原子第一电离能大 根据原子核外电子排布的特点,Cu在周期表中属于s区元素
因氧元素电负性比氮元素大,故氧原子第一电离能比氮原子第一电离能大 根据原子核外电子排布的特点,Cu在周期表中属于s区元素
 因氧元素电负性比氮元素大,故氧原子第一电离能比氮原子第一电离能大 根据原子核外电子排布的特点,Cu在周期表中属于s区元素
因氧元素电负性比氮元素大,故氧原子第一电离能比氮原子第一电离能大 根据原子核外电子排布的特点,Cu在周期表中属于s区元素
 因氧元素电负性比氮元素大,故氧原子第一电离能比氮原子第一电离能大 根据原子核外电子排布的特点,Cu在元素周期表中位于s区
因氧元素电负性比氮元素大,故氧原子第一电离能比氮原子第一电离能大 根据原子核外电子排布的特点,Cu在元素周期表中位于s区
 O 氯原子的结构示意图:
O 氯原子的结构示意图: Fe3+的最外层电子排布式为3s23p63d5 基态铜原子的外围电子排布图:
Fe3+的最外层电子排布式为3s23p63d5 基态铜原子的外围电子排布图: 
 因氧元素电负性比氮元素大,故氧原子第一电离能比氮原子第一电离能大 根据原子核外电子排布的特点,Cu在周期表中属于s区元素
因氧元素电负性比氮元素大,故氧原子第一电离能比氮原子第一电离能大 根据原子核外电子排布的特点,Cu在周期表中属于s区元素
 O. 氯原子的结构示意图:
O. 氯原子的结构示意图: Fe3+的最外层电子排布式为3s23p63d5 基态铜原子的外围电子排布图:
Fe3+的最外层电子排布式为3s23p63d5 基态铜原子的外围电子排布图:
 它违背了泡利原理 Xe元素的所在族的原子的外围电子排布式均为ns2np6,属于非金属元素
它违背了泡利原理 Xe元素的所在族的原子的外围电子排布式均为ns2np6,属于非金属元素
 某基态原子外围电子的核外电子排布图为 它违背了泡利原理 Xe元素的所在族的原子的外围电子排布式均为ns2np6,属于非金属元素
某基态原子外围电子的核外电子排布图为 它违背了泡利原理 Xe元素的所在族的原子的外围电子排布式均为ns2np6,属于非金属元素
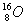 氯原子的结构示意图:
氯原子的结构示意图: 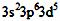 Fe3+的最外层电子排布式为:
Fe3+的最外层电子排布式为:  基态铜原子的外围电子排布图为:
基态铜原子的外围电子排布图为: