你可能感兴趣的试题
254g I2(g)中通入2gH2(g),反应放热9.48 kJ 1 mol固态碘与1 mol气态碘所含的能量相差17.00 kJ 反应(i)的产物比反应(ii)的产物稳定 反应(ii)的反应物总能量比反应(i)的反应物总能量低
H2、I2、HI的浓度相等 H2、I2、HI的浓度保持不变 混合气体的密度保持不变 混合气体的质量不再改变
该反应的正反应是吸热反应 该反应的逆反应是放热反应 该反应的正反应是放热反应 温度对该反应无影响
H2(g)的消耗速率与HI(g)的生成速率比为21 反应进行的净速率是正、逆反应速率之差 正、逆反应速率的比值是恒定的 达到平衡时,正、逆反应速率相等
反应正好达平衡 反应向左进行 反应向某方向进行一段时间后K<57.0 反应向某方向进行一段时间后c(H2)<0.2 mol·L-1
恒容时,升高温度,平衡向逆反应方向移动,正反应速率减小 恒温时,减小容积平衡不移动,但气体颜色加深 恒容时,通入H2,则I2的质量分数减小 恒压时,通入HI气体,刚开始时正反应速率会减小
0.2mol HI充分分解,吸收1.25kJ热量 加入催化剂,Ea减小,△H.不变 其他条件不变,升高温度,反应速率加快,HI分解率不变 其他条件不变,增大压强,反应速率加快,HI分解率增大 
正、逆反应速率都等于零 HI、H2、I2的浓度相等 HI、H2、I2在容器中共存 HI、H2、I2的浓度均不再变化
0.2mol HI充分分解,吸收1.25kJ热量 加入催化剂,Ea减小,△H.不变 其他条件不变,升高温度,反应速率加快,HI分解率不变 其他条件不变,增大压强,反应速率加快,HI分解率增大 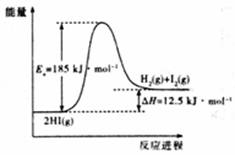
c(H2)保持不变 拆开2 molH.-I.共价键,同时生成1 molH.-H.共价键 HI、H2、I2的浓度比为2:1:1 正反应和逆反应都已停止


