你可能感兴趣的试题
m>p,正反应为放热反应 mm+n>p,正反应为放热反应 m+n>p,正反应为吸热反应
K越大,达到平衡时,反应进行的程度越小 K越小,达到平衡时,反应物的转化率越大 K随反应物浓度改变而改变 K随温度改变而改变
K.值越大,表明该反应速率越快,反应物的转化率也越大 若缩小反应器的容积,能使平衡正向移动,则K.增大 温度相同,K.值也一定相同。 pC(g)  mA(g)+nB(g) 的平衡常数与K.互为相反数。
mA(g)+nB(g) 的平衡常数与K.互为相反数。
到达平衡后,若使用催化剂,C.的质量分数增大 平衡后,若升高温度,平衡则向逆反应 方向移动 平衡后增大A.的量,有利于提高A.的转化率 化学方程式中一定
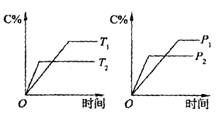
的转化率同压强、温度的关系,分析图像结论正确是 A.正反应吸热,m+n>p+q 正反应吸热,m+n正反应放热,m+n > p+q 正反应放热,m+n < p+q
平衡常数发生变化,化学平衡必发生移动 化学平衡发生移动,平衡常数必发生变化 反应物的转化率越大,达到平衡时,K.值越大 温度越高,达到平衡时,K.值越大
的转化率同压强、温度的关系,分析图像结论正确是 A.正反应吸热,m+n>p+q 正反应吸热,m+n正反应放热,m+n > p+q 正反应放热,m+n < p+q
m>p,正反应为放热反应 mm+n>p,正反应为放热反应 m+n>p,正反应为吸热反应
降温,化学平衡向正反应方向移动
使用催化剂可使D.%有所增加
化学方程式中气体的化学计量数m<p+q
B.的颗粒越小,正反应速率越快,有利于平衡向正反应方向移动。
K越大,达到平衡时,反应进行的程度越小 K越小,达到平衡时,反应物的转化率越大 K随反应物浓度改变而改变 K随温度改变而改变
K.越大,达到平衡时,反应进行的程度越大 K.越小,达到平衡时,反应物的转化率越大 K.随反应物浓度的改变而改变 K.随温度和压强的改变而改变

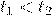
两图中阴影部分面积相等 图Ⅱ中阴影部分面积更大
增加A.的量,平衡正向移动,达到新平衡时K.值增大 升高温度,K.值增大 K.越大,说明该反应的进行程度越大,转化率越高 该反应的K.=

 mA(g)+nB(g) 的平衡常数与K.互为相反数。
mA(g)+nB(g) 的平衡常数与K.互为相反数。