你可能感兴趣的试题
CCl4与I2分子量相差较小,而H2O与I2分子量相差较大 CCl4与I2都是直线型分子,而H2O不是直线型分子 CCl4和I2都不含氢元素,而H2O中含有氢元素 CCl4和I2都是非极性分子,而H2O是极性分子
NH3是极性分子,分子中N.原子处在3个H.原子所组成的三角形的中心 CCl4是非极性分子,分子中 原子处在4个Cl原子所组成的正方形的中心C.CO2是非极性分子,分子中C.原子不处在2个O.原子所连的直线的中央 H2O是极性分子,分子中O.原子不处在2个H.原子所连成的直线的中央
NH3是极性分子,分子中N.原子处在3个H.原子所组成的三角形的中心 CCl4是非极性分子,分子中 原子处在4个Cl原子所组成的正方形的中心 C. H2O是极性分子,分子中O.原子不处在2个H.原子所连成的直线的中央 CO2是非极性分子,分子中C.原子不处在2个O.原子所连成的直线的中央
NH3是极性分子,分子中N.原子是在3个H.原子所组成的三角形的中心 CCl4是非极性分子,分子中 原子处在4个Cl原子所组成的正方形的中心 C.H2O是极性分子,分子中O.原子不处在2个H.原子所连成的直线的中央 CO2是非极性分子,分子中C.原子不处在2个O.原子所连成的直线的中央
B.两种纯液体流,根据图分析,这两种液体分子的极性正确的是( )  A.A.是极性分子, 是非极性分子 B.A.是非极性分子,B.是极性分子 A.和B.都是极性分子 A.和B.都是非极性分子
A.A.是极性分子, 是非极性分子 B.A.是非极性分子,B.是极性分子 A.和B.都是极性分子 A.和B.都是非极性分子
CO2是直线形分子,CO2是非极性分子
H2O是具有极性共价键的极性分子
NH3是具有极性共价键的非极性分子
若H―O―O―H分子是极性分子,则H―O―O―H分子一定不是直线形分子
CCl4与I2分子量相差较小,而H2O与I2分子量相差较大 CCl4与I2都是直线型分子,而H2O不是直线型分子 CCl4和I2都不含氢元素,而H2O中含有氢元素 CCl4和I2都是非极性分子,而H2O是极性分子www.jk.zy.w.com
C60和NO2都是共价化合物 CCl4和NH3都是以极性键结合的极性分子 在NaCl和SiO2晶体中,都不存在单个小分子 甲烷的结构式: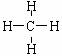 ,是对称的平面结构,所以是非极性分子
,是对称的平面结构,所以是非极性分子
多原子分子中,键的极性越强,分子的极性也越强 具有极性共价键的分子一定是极性分子 非极性分子中的化学键一定是非极性共价键 双原子分子中的键是非极性键,分子一定是非极性分子
P4和NO2都是共价化合物 CCl4和NH3都是以极性键结合的极性分子 在CaO和SiO2晶体中,都不存在单个小分子 甲烷的结构式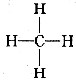 是对称的平面结构,所以是非极性分子
是对称的平面结构,所以是非极性分子
NH3是极性分子,分子中N.原子是在3个H.原子所组成的三角形的中心 CCl4是非极性分子,分子中 原子处在4个Cl原子所组成的正方形的中心C. H2O是极性分子,分子中O.原子不处在2个H.原子所连成的直线的中央 CO2是非极性分子,分子中C.原子不处在2个O.原子所连成的直线的中央
在水中能电离出离子的化合物一定是离子化合物 CO2分子中含极性键,且溶于水能导电,所以CO2是电解质 Ca(OH)2微溶于水,所以是弱电解质 CH3COOH在水中只能部分电离,所以是弱电解质
NH3是极性分子,分子中N原子处在3个H原子所组成的三角形的中心 CCl4是非极性分子,分子中C原子处在4个Cl原子所组成的正方形的中心 H2O是极性分子,分子中O原子不处在2个H原子所连成的直线的中央 CO2是非极性分子,分子中C原子不处在2个O原子所连成的直线的中央
①⑥为极性分子,②③④⑤为非极性分子 只有④为非极性分子,其余为极性分子 只有②⑤是极性分子,其余为非极性分子 只有①③是非极性分子,其余是极性分子
钻石表面表现为非极性,水是极性分子 钻石表面表现为非极性,水是非极性分子 钻石表面表现为极性,水是非极性分子 钻石表面表现为极性,水是极性分子
 A.A.是极性分子, 是非极性分子 B.A.是非极性分子,B.是极性分子 A.和B.都是极性分子 A.和B.都是非极性分子
A.A.是极性分子, 是非极性分子 B.A.是非极性分子,B.是极性分子 A.和B.都是极性分子 A.和B.都是非极性分子
 ,是对称的平面结构,所以是非极性分子
,是对称的平面结构,所以是非极性分子
 是对称的平面结构,所以是非极性分子
是对称的平面结构,所以是非极性分子