你可能感兴趣的试题
原NaOH溶液的物质的量浓度为0.5 mol/L 当0盐酸)<10 mL时,甲溶液中发生反应的离子方程式为H++CO32-=HCO3- 乙溶液中含有的溶质是Na2CO3、NaOH 向乙溶液中滴加过量盐酸后产生CO2体积的最大值为224 mL
和 :A.为盐酸,B.为醋酸。分别和锌反应,若最后仅有一份溶液中存在锌,且放出的氢气的质量相等,则下列说法正确的是 ① 反应所需要的时间B.>A ② 开始反应时的速率A.>B ③ 参加反应的锌的物质的量A.=B.④ 反应过程的平均速率B.>A ⑤ 盐酸里有锌剩余 ⑥ 醋酸里有锌剩余 A. ③④⑤B.③④⑥ ②③⑤ ②③⑤⑥
和 ;A.为盐酸,B.为醋酸,分别和锌反应,若最后仅有一份溶液中存在锌,且放出的氢气的质量相等,则下列说法正确的是( ) ①反应所需要的时间B.>A②开始反应时的速率A.>B③参加反应的锌的物质的量A.=B.④反应过程的平均速率B.>A⑤盐酸里有锌剩余⑥醋酸里有锌剩余 A.③④⑤ B.③④⑥ ②③⑤ ②③⑤⑥
原NaOH溶液的物质的量浓度为0.5 mol·L-1 当0-+H+=H2O 乙溶液中含有的溶质是Na2CO3、NaHCO3 乙溶液中滴加盐酸后产生CO2体积的最大值为224mL(标准状况)
乙溶液中含有的溶质是NaOH、NaHCO3 当0-+ H.+ ===H2O 原NaOH溶液的物质的量浓度为0.5 mol·L-1 乙溶液中滴加盐酸后产生CO2体积的最大值为112 mL(标准状况)
原NaOH溶液的物质的量浓度为0.5 mol/L 当0盐酸)<10 mL时,甲溶液中发生反应的离子方程式为H++CO32-=HCO3- 乙溶液中含有的溶质是Na2CO3、NaOH 向乙溶液中滴加过量盐酸后产生CO2体积的最大值为224 mL
和 ;A.为盐酸,B.为醋酸,分别和锌反应,若最后仅有一份溶液中存在锌,且放出的氢气的质量相等,则下列说法正确的是( ) ①反应所需要的时间B.>A②开始反应时的速率A.>B③参加反应的锌的物质的量A.=B.④反应过程的平均速率B.>A⑤盐酸里有锌剩余⑥醋酸里有锌剩余 A.③④⑤ B.③④⑥ ②③⑤ ②③⑤⑥
原NaOH溶液的物质的量浓度为0.5 mol·L-1 当0-+H+=H2O 乙溶液中含有的溶质是Na2CO3、NaHCO3 乙溶液中滴加盐酸后产生CO2体积的最大值为224mL(标准状况)
和 ,A.为盐酸,B.为醋酸,分别和锌反应,若最后仅有一份溶液中存在锌,且放出氢气的质量相同,则下列说法正确的是( ) ①反应所需的时间B.>A ②开始反应时的速率为A.>B ③加入锌的物质的量A.>B ④反应过程中的平均速率为B.>A ⑤盐酸里有锌剩余 ⑥醋酸里有锌剩余 A.③④⑤ B.③④⑥ ②③⑤ ②③⑤⑥
1 mol/L的NaHA溶液,其pH=4:c(HA-)>c(H+)>c(H2A.)>c(A2-) 有甲、乙两醋酸溶液,测得甲的pH=a,乙的pH=a+1,若用于中和等物质的量浓度等体积的NaOH溶液,需甲、乙两酸的体积V. (乙)>10V.(甲) 常温下中和等体积、pH相同的CH3COOH和HCl溶液,消耗NaOH的量相同 将pH=3的醋酸稀释为pH=4的过程中,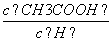 比值不变
比值不变
乙溶液中滴加盐酸后产生CO2体积的最大值为112mL(标准状况) 当0-+H+→H2O 乙溶液中含有的溶质是NaOH、NaHCO3 原NaOH溶液的物质的量浓度为0.5 mol·L-1
金属是镁,甲溶液为0.2 mol/L盐酸,乙溶液为0.1 mol/L盐酸 金属是铁,甲溶液为pH=1的醋酸溶液,乙溶液为pH=1的盐酸 金属是铝,甲溶液为0.1 mol/L盐酸,乙溶液为0.1 mol/L氢氧化钠溶液 金属是铝,甲溶液为0.1mol/L氢氧化钠溶液,乙溶液为0.1 mol/L盐酸
和 ,A.为盐酸,B.为醋酸,分别和锌反应,若最后仅有一份溶液中存在锌,且放出的氢气的体积相等,则下列说法正确的是( ) ①反应所需要的时间B.>A.②开始反应时的速率A.>B.③参加反应的锌的物质的量A.=B. ④反应过程的平均速率B.>A ⑤盐酸里有锌剩余 ⑥醋酸里有锌剩余 A.③④⑤B.③④⑥ ②③⑤ ②③⑥

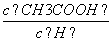 比值不变
比值不变
