你可能感兴趣的试题
CO32-和SO42-一定不存在于溶液X.中 沉淀甲是硅酸和硅酸镁的混合物 K+、AlO2-和SiO32-一定存在于溶液X.中 气体甲一定是纯净物
K+、Na+、NO3-、SiO32- K+、Na+、Ba2+、SO42- K+、Ca2+、Na+、CO32﹣ H+、NH4+、K+、Cl-
X 中肯定存在 Fe2+、Al3+、NH4+、SO42- X.中不能确定是否存在的离子是Al3+和Cl- 溶液E.和气体F.发生反应,生成物为盐类 气体A.是NO
K+ SO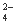 Ba2+ NH
Ba2+ NH
以MnO2为原料制得的MnCl2溶液中常含有Cu2+等金属离子,通常添加难溶电解质MnS使这些离子形成硫化物沉淀而除去:Cu2+ + S2-=CuS↓ 盛放NaOH溶液的试剂瓶不能用玻璃塞:SiO2 + 2OH- = SiO32- + H2O 金属钠在空气中放置表面会很快失去金属光泽:2Na + O2 = Na2O2 向硫酸亚铁铵[(NH4)2Fe(SO4) 2·6H2O]的稀溶液中加入足量Ba(OH)2稀溶液:NH4+ + Fe2+ + SO42-+ Ba2+ +3OH- = BaSO4↓+ Fe(OH)2↓+ NH3·H2O
原溶液中存在NH4+、Fe2+、Cl-、SO42- 滤液X.中大量存在的阳离子有NH4+、Fe2+和Ba2+ 无法确定沉淀C.的成分 无法确定原试液中是否含有Al3+、Cl-
Ca2+、Al3+、Ag+ Al3+、Ag+、Ba2+ Ag+、Mg2+、Ca2+ Ag+、Ba2+、Mg2+
13+、Mg2+、A.1O2-、CO32-、SiO32-、C.1-中的几种,现进行如下实验: ①取少量溶液加氢氧化钠溶液过程中无沉淀生成; ②另取少量原溶液,逐滴加入5 mL 0.2 mol • L-1的盐酸,发生的现象是开始产生沉淀并逐渐增多,沉淀量基本不变后产生气体,最后沉淀逐渐减少至消失; ③在上述②沉淀消失后的溶液中,再加入足量的硝酸银溶液可得到沉淀0.435 g。 下列说法中正确的是 A.该溶液中一定不含有Ba2+、Mg2+、A.13+、SiO32-、C.1- 该溶液中一定含有K+、A.1O2-、CO32-、 1- C.该溶液中是否含有K+需做焰色反应(透过蓝色钴玻璃片) 可能含有C.1-
向Na2SiO3溶液中逐滴加入少量稀盐酸:SiO32-+ 2H+=H2SiO3(胶体) 向Na2S2O3溶液中加入稀硫酸:2S2O32-+2H+=SO42-+3S↓+H2O 将Cu片加入稀硝酸中:3Cu + 8H++2NO3-=3Cu2+ +2NO↑+ 4H2O 向NH4Al(SO4)2溶液中加入过量的Ba(OH)2稀溶液: NH4+ + Al3+ + 2SO42- + 2Ba2+ + 5OH-=2BaSO4↓+ NH3·H2O + AlO2-+ 2H2O

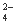 Ba2+ NH
Ba2+ NH