你可能感兴趣的试题
生物利用度是指剂型中的药物被吸收进入血液的速率和程度 生物利用度是指一种药物的不同制剂在相同的试验条件下,给以相同的剂量,反映其吸收速率和程度的主要动力学参数没有明显的统计学差异 生物等效性是指剂型中的药物被吸收进入血液的速率和程度 生物等效性是指一种药物的不同制剂在相同的试验条件下,给以相同的剂量,反映其吸收速率和程度的主要动力学参数没有明显的统计学差异 生物利用度有绝对生物利用度和相对生物利用度之分 化学药品属注册分类6中的口服固体制剂应当进行生物等效性试验
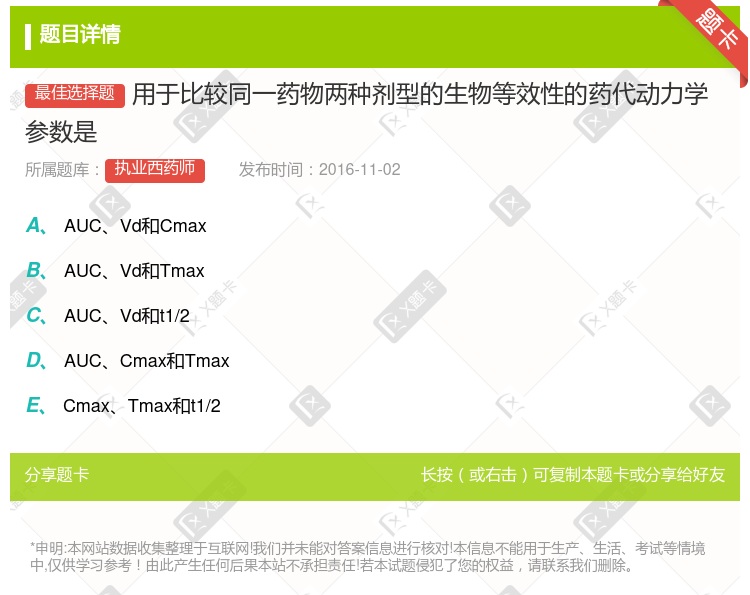
AUC、Vd和Cmax AUC、Vd和Tmax AUC、Vd和t1/2 AUC、Cmax和Tmax Cmax、Tmax和t1/2
药物剂型或给药途径改变,半衰期也随之改变 药物的水溶性越大,表观分布容积越大 对于消除过程具有零级动力学的药物而言,其生物半衰期随剂量的增加而延长 亲脂性药物在肥胖者体内的表观分布容积较正常者小 速率常数越大,表明药物半衰期越长
AUC、Vd和Cmax AUC、Vd和T1/2 AUC、Vd和t1/2 AUC、Cmax和Tmax AUC、K和tl/2
AUC、Vd、C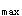 AUC、Vd、t
AUC、Vd、t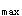 AUC、Vd、t
AUC、Vd、t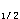 AUC、C
AUC、C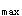 、t
、t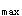 C
C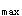 、t
、t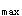 、t
、t
生物半衰期(t1/2) 清除率(Cl) 血药峰浓度(Cmax) 表现分布容积(V) 血药浓度-时间曲线下面积(AU
房室模型为药物固有的药代动力学指标 多数药物按单房室模型转运 药代动力学房室是按药物转运速率以数学方法划分的概念 用同一药物试验,在某些人呈二室模型,而在某些人可呈单室模型 同一药物口服时呈二室模型而静脉注射则可呈单一房室模型
开展生物等效性试验的,应当报国家药品监督管理局药品审评中心批准 一般仿制药的研制需要进行生物等效性试验 原则上,企业应采用体内生物等效性试验的方法进行仿制药质量和疗效一致性评价 生物等效性试验用样品的处方、工艺、生产线应与商业化生产保持一致
生物半衰期(t+1/2) 清除率(CI) 血药峰浓度(Cmax) 表现分布容积(V) 血药浓度-时间曲线下面积(AUC)
测定血液或其他体液中的药物浓度 临床药代动力学研究 人体生物利用度研究 人体生物等效性研究 必要时根据药代动力学原理调整给药方案
药代动力学房室模型是按药物分布速度以数学方法划分的概念 多数药物按单房室模型转运 房室模型为药物固有的药代动力学指标 用同一药物试验,在某些人呈二室模型,而在某些人可呈单室模型 同一药物口服时呈二室模型而静脉注射则可呈单一房室模型
研究制剂的生物利用度,定量解释和比较制剂的内在质量 应用药物动力学参数设计临床给药方案 探讨药物结构与药物动力学规律的关系,开发新药;指导制剂设计与生产 探讨体外药物动力学特征(溶出度)与体内药物动力学特征的关系, 建立药物动力学模型,测定药动学参数
动物药代动力学试验 生物等效性试验和临床试验 临床试验 药物稳定性、药理和毒理 生物等效性试验
生物等效性研究方法的优先顺序常为药代动力学研究、药效动力学研究、临床研究和体外研究 用于评价生物等效性的药动学指标包括Cmax和AUC 仿制药生物等效性试验应尽可能选择原研产品作为参比制剂 对于口服常释制剂,通常需进行空腹和餐后生物等效性研究 筛选受试者时的排除标准应主要考虑药效
生物利用度是指剂型中的药物被吸收进入血液的速率和程度 生物利用度是指一种药物的不同制剂在相同的试验条件下,给以相同的剂量,反映其吸收速率和程度的主要动力学参数没有明显的统计学差异 生物等效性是指剂型中的药物被吸收进入血液的速率和程度 生物等效性是指一种药物的不同制剂在相同的试验条件下,给以相同的剂量,反映其吸收速率和程度的主要动力学参数没有明显的统计学差异 生物利用度有绝对生物利用度和相对生物利用度之分 化学药品属注册分类6中的口服固体制剂应当进行生物等效性试验
两种含同一有效成分的制剂,生物利用度不同 两种剂型相同而含不同有效成分的药品,效应相同 两种剂型相同而所含药物剂量不同的药物,作用相同 两种剂型相同而含同一有效成分的药品,效应不同 两种药学等效的制剂,所含有效成分的生物利用度相同
临床试验 生物等效性试验 临床试验和生物等效性试验 药理、毒理试验 动物药代动力学试验
药代动力学房室模型是按药物分布速度以数学方法划分的概念 多数药物按单房室模型转运 房室模型为药物固有的药代动力学指标 用同一药物试验,在某些人呈二室模型,而在某些人可呈单室模型 同一药物口服时呈二室模型而静脉注射则可呈单一房室模型
生物半衰期(t1/2) 清除率(Cl) 血药峰浓度(Cmax) 表观分布容积(V) 血药浓度一时间曲线下面积(AUC)
AUC、V和Cmax AUC、V和tmax AUC、V和t1/2 AUC、Cmax和tmax AUC、tmax和t1/2
 AUC、Vd、t
AUC、Vd、t AUC、Vd、t
AUC、Vd、t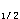 AUC、C
AUC、C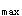 、t
、t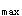 C
C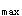 、t
、t 、t
、t