你可能感兴趣的试题
5%Na2CO3、1%NaOH、5%NaOH、5%NaHCO3 5%NaOH、1%NaOH、5%Na2CO2、5%NaHCO3 5%NaHCO3、5%Na2CO3、1%NaOH、5%NaOH 5%Na2CO3、1%NaOH、5%NaHCO3、5%NaOH 5%NaHCO3、5%Na2CO3、5%NaOH、1%NaOH
向含有CaCO3沉淀的水中通入CO2至沉淀恰好溶解,再向溶液中加入NaHCO3饱和溶液, 又有CaCO3沉淀生成 向Na2 CO3溶液中逐滴加入等物质的量的稀盐酸,生成的CO2与原溶液中Na2CO3的物质 的量之比为1:2 等质量的NaHCO3和Na2 CO3分别与足量稀盐酸反应,在同温同压下,生成的CO2体积相同 向Na2CO3饱和溶液中通入足量CO2,有NaHCO3 结晶析出
等浓度的溶液中滴入稀盐酸,放出气体的快慢Na2CO33 热稳定性Na2CO33 常温时水溶性Na2CO33 相对分子质量Na2CO33
碳碳键键长:乙烯>苯 密度:一氯乙烷>一氯丁烷 热稳定性: NaHCO3>Na2CO3>H2CO3 沸点:H2O>H2S>H2Se
和酸反应放出等量的CO2所消耗的酸比Na2CO3少 相同温度下溶解度比NaCO3要大 热稳定性比Na2CO3小 NaHCO3只能和酸作用不能和碱作用
pH = a的氨水溶液,稀释10倍后,其pH = b,则a = b + 1 向NaAlO2溶液中滴加NaHCO3溶液,有沉淀和气体生成 在Na2C2O4稀溶液中,c(OH-) = c(H+) + c(HC2O4—) + 2c(H2C2O4) 0.1 mol/L Na2CO3溶液与0.1 mol/L NaHCO3溶液等体积混合: 3c(Na+) = 2[c(CO32—) + c(HCO3—) + c(H2CO3) ]
对热稳定性:Na2CO3 >NaHCO3 常温时水溶性:Na2CO3 >NaHCO3 与稀盐酸反应的快慢:Na2CO3 >NaHCO3 相对分子质量:Na2CO3>NaHCO3
热稳定性:Na2CO3 < NaHCO3 常温时水溶性:Na2CO3 > NaHCO3 与稀盐酸反应速率:Na2CO3 < NaHCO3 相对分子质量:Na2CO3 < NaHCO3
工业上通过电解熔融状态MgCl2制取金属镁 用澄清的石灰水可鉴别NaHCO3和Na2CO3 在第②、④步骤中,溴元素均被氧化 制取NaHCO3的反应是利用其溶解度小于NaCl
溶解度:NaHCO3 > Na2CO3 酸性:H2SiO3 > H2CO3 熔点:金刚石 > 晶体硅 热稳定性:NaHCO3 > Na2CO3
酸性HY>HX 结合H+的能力Y->CO >X->HCO
>X->HCO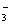 溶液的碱性:NaX>Na2CO3>NaY>NaHCO3 HX和HY酸性相同但比H2CO3弱
溶液的碱性:NaX>Na2CO3>NaY>NaHCO3 HX和HY酸性相同但比H2CO3弱
放Na2CO3的一端托盘下沉 放NaHCO3的端托盘下沉 仍保持平衡 无法判断
对热稳定性:Na2CO3<NaHCO3 常温时水溶性:Na2CO3>NaHCO3 与稀盐酸反应的快慢:Na2CO3>NaHCO3 相对摩尔质量:Na2CO3< NaHCO3

 >X->HCO
>X->HCO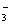 溶液的碱性:NaX>Na2CO3>NaY>NaHCO3 HX和HY酸性相同但比H2CO3弱
溶液的碱性:NaX>Na2CO3>NaY>NaHCO3 HX和HY酸性相同但比H2CO3弱