你可能感兴趣的试题
为了选择Ⅱ和Ⅲ实验探究硫酸铜对反应速率的影响,必须控制t=25 待测物理量是收集等体积(相同条件)气体所需要的时间,时间越长,反应越快 根据该方案,还可以探究硫酸浓度对反应速率的影响 根据该实验方案得出反应速率大小可能是Ⅲ>Ⅱ>Ⅰ>Ⅳ
①稀硫酸 ②硫酸铜 ①稀盐酸 ②硫酸锌 ①稀盐酸 ②硫酸亚铁 ①稀硫酸 ②氯化镁
加入几滴硫酸铜溶液 加入适量的水 加入适量镁粉 再加入少量稀硫酸
对比实验①和③,探究硫酸的浓度对该反应剧烈程度的影响 对比实验②和③,探究硫酸的浓度对该反应剧烈程度的影响 对比实验①和③,探究温度对该反应剧烈程度的影响 对比实验②和③,探究温度对该反应剧烈程度的影响
升高溶液的温度 初始加入的稀硫酸由5 mL变成10 mL 将锌块换成锌粉 加几滴硫酸铜溶液
加入少量稀硫酸 加热 加蒸馏水 加入少量硫酸铜溶液
升高温度,可以加快反应速率,缩短可逆反应达到平衡的时间 化学反应达到最大限度时,正逆反应速率也达到最大且相等 用锌和稀硫酸反应制取H2时,滴加几滴硫酸铜溶液能加快反应速率 用铁片和稀硫酸反应制H2比用98%的浓硫酸产生H2的速率快
对比实验①和③,研究硫酸的浓度对反应剧烈程度的影响 对比实验②和③,研究硫酸的浓度对反应剧烈程度的影响 对比实验①和③,研究温度对反应剧烈程度的影响 对比实验①和②,研究温度对反应剧烈程度的影响
实验①、②说明锌能与稀硫酸反应而铜不能 实验③说明发生原电池反应时会加快化学反应速率 实验③说明在该条件下铜可以与稀硫酸反应生成氢气 实验④说明该原电池中铜为正极、锌为负极
①稀硫酸②硫酸铜 ①稀盐酸②硫酸锌 ①稀盐酸②硫酸亚铁 ①稀硫酸②氯化镁 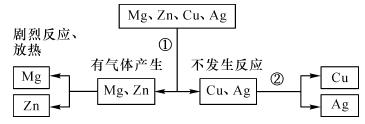
加入少量硫酸铜溶液 加入少量氯化锌溶液 把纯锌换成有铜杂质的锌 把稀硫酸换成浓硫酸

