你可能感兴趣的试题
转移0.1mol电子时,a电极产生1.12LH2(标准状况) b电极上发生的电极反应是: 2H2O+2e-=H2↑+2OH- c电极上进行还原反应,B.电池中的H+可以通过隔膜进入A.池 d电极上发生的电极反应是:O2+4H++4e-=2H2O
当有0.1mol电子转移时,a极产生1.12L O2(标准状况下) b极上发生的电极反应是:4H2O + 4e- = 2H2↑+ 4OH- d极上发生的电极反应是:O2 + 4H+ + 4e- = 2H2O c极上发生还原反应,B.中的H+可以通过隔膜进入A.室
B.区的OH-通过隔膜向a电极移动,A区pH增大 图中右管中的OH-通过隔膜向c电极移动,d电极上发生还原反应 c是正极,电极上的电极反应为:  当有1mol电子转移时,b电极产生气体Y.的体积为11.2L
当有1mol电子转移时,b电极产生气体Y.的体积为11.2L
当有0.1mol电子转移时,a极产生1.12L O2(标准状况下) b极上发生的电极反应是:4H2O + 4e- = 2H2↑+ 4OH- d极上发生的电极反应是:O2 + 4H+ + 4e- = 2H2O c极上进行还原反应,B.中的H+可以通过隔膜进入A.
当有0.1mol电子转移时,a 极产生1.12L气体 b极上发生的电极反应是:4H2O+4e-=2H2↑+4OH– c 极上发生还原反应,B.中的H+ 可以通过隔膜进入A. d 极上发生的电极反应是:O2+4H++4e-=2H2O
当d极消耗2g H2 时,a极周围会产生22.4L H2
电解时,电子流动路径是:负极→外电路→阴极→溶液→阳极→正极
c极上发生的电极反应是:O2+2H2O+4e﹣=4OH﹣
c极上进行还原反应,B中的H+可以通过隔膜进入A
当转移0.1 mol电子,a极产生2.24L. H2 b电极反应是:4H2O +4e-=2H2↑+4OH— d电极反应是:O2 +4H+ +4e-=2H2O c极上发生还原反应,B.中H+经隔膜进入A. 
当有0.1mol电子转移时,a极产生1.12L O2(标准状况下) b极上发生的电极反应是:4H2O + 4e- = 2H2↑+ 4OH- d极上发生的电极反应是:O2 + 4H+ + 4e- = 2H2O c极上进行还原反应,B.中的H+可以通过隔膜进入A. 
当转移0.1 mol电子,a极产生2.24L. H2 b电极反应是:4H2O +4e-=2H2↑+4OH— d电极反应是:O2 +4H+ +4e-=2H2O c极上发生还原反应,B.中H+经隔膜进入A. 
当有0.1 mol电子转移时,a极产生1.12L. O2(标准状况下) b极上发生的电极反应是:4H2O+4e-==2H2↑+4OH- c极上发生的电极反应是:O2+4H++4e-==2H2O d极上进行还原反应,产生的H.+可以通过隔膜进入A.
图中右管中的OH-通过隔膜向c电极移动,d电极上发生还原反应 B.区的OH-通过隔膜向a电极移动,A.区pH增大 c是正极,电极上的电极反应为2H++2e-===H2↑ 当有1 mol电子转移时,b电极产生气体Y.的体积为11.2L.
图中右管中的OH-通过隔膜向c电极移动,d电极上发生还原反应 B.区的OH-通过隔膜向a电极移动,A.区pH增大 c是正极,电极上的电极反应为2H++2e-===H2↑ 当有1 mol电子转移时,b电极产生气体Y.的体积为11.2L.
当有0.1mol电子转移时,a极产生1.12L O2(标准状况下) b极上发生的电极反应是:4H2O + 4e- = 2H2↑+ 4OH- d极上发生的电极反应是:O2 + 4H+ + 4e- = 2H2O c极上进行还原反应,B.中的H+可以通过隔膜进入A.
当有0.1 mol电子转移时,a极产生 0.56L. O2(标准状况下) 左端装置中化学能转化为电能,右端装置中电能转化为化学能 d极上发生的电极反应是:O2 + 4H+ + 4e- 2H2O c极上进行还原反应,右端装置B.中的H+可以通过隔膜进入A. 
当有0.1mol电子转移时,a电极产生1.12LH2(标准状况下) b电极上发生的电极反应是: 4H2O+4e-=2H2↑+4OH- c电极上进行的是氧化反应,B池中的H+可以通过隔膜进入A.池 d电极上发生的电极反应是: O2+4H++4e-=2H2O 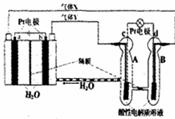
图甲把化学能转化为电能,图乙把电能转化为化学能,水得到了循环使用 当有0.1 mol电子转移时,a极产生0.56 L O2(标准状况下) c极上发生的电极反应是O2+4H++4e-===2H2O 图乙中电子从c极流向d极,提供电能
转移0.1mol电子时,a电极产生1.12LH2(标准状况) b电极上发生的电极反应是: 2H2O+2e-=H2↑+2OH- c电极上进行还原反应,B.电池中的H+可以通过隔膜进入A.池 d电极上发生的电极反应是:O2+4H++4e-=2H2O
当有0.1mol电子转移时,a电极产生0.56L气体(标准状况下) b电极上发生的电极反应是: 4H2O+4e-=2H2↑+4OH- c电极上进行还原反应,B.电池中的H+可以通过隔膜进入A.池 d电极上发生的电极反应是:O2+4H++4e-=2H2O

 当有1mol电子转移时,b电极产生气体Y.的体积为11.2L
当有1mol电子转移时,b电极产生气体Y.的体积为11.2L





