你可能感兴趣的试题
在一定浓度下,平衡常数值越大则酸的电离度也越大 在一定浓度下,平衡常数值越大则酸的电离度越小 平衡常数值越大则溶液的浓度越大 平衡常数值越大则溶液的浓度越小
电离平衡常数能衡量电解质电离的相对强弱 电离平衡常数不随浓度变化而变化 电离平衡常数与温度有关 电离平衡常数不随任何条件而改变
电离平衡常数越小,表示弱电解质的电离能力越弱 电离平衡常数与温度无关 不同浓度的同一弱电解质,其电离平衡常数不同 多元弱酸各步电离平衡常数相互关系为:K1〈K2〈K3
对于弱电解质,电离平衡常数不因浓度改变而改变,但随温度改变而改变 弱电解质的电离平衡常数愈大,电解质愈易电离 电离平衡常的大小反映了弱电解质的相对强弱 对于弱电解质,电离平衡常数随浓度改变而
在一定浓度下,平衡常数值越大则碱的电离度也越大 在一定浓度下,平衡常数值越大则碱的电离度越小 平衡常数值越大则溶液的浓度越大 平衡常数值越大则溶液的浓度越小
不同浓度的同一弱电解质,其电离平衡常数(K.)不同 电离平衡常数(K.)越小,表示弱电解质电离能力越弱 多元弱酸各步电离平衡常数相互关系为:K.1<K.2<K.3 CH3COOH溶液中加入少量CH3COONa溶液,电离常数减小
化学反应速率v 化学平衡常数K. 水的离子积常数Kw 弱酸的电离常数Ka
CH3COONa NaClO Na2CO3 Na3PO4
在一定浓度下,平衡常数值越大则酸的电离度也越大 在一定浓度下,平衡常数值越大则酸的电离度越小 平衡常数值越大则溶液的浓度越大 平衡常数值越大则溶液的浓度越小
一定温度下,弱酸的电离常数越大,酸性越强 醋酸的电离常数Ka和醋酸钠的水解常数Kh之间的关系为:Ka·Kh=Kw 溶度积越小,该物质一般越容易在溶液中形成沉淀 合成氨的反应,正反应的平衡常数和逆反应的平衡常数相同。
电离平衡常数能衡量电解质电离的相对强弱 电离平衡常数不随浓度变化而变化 电离平衡常数与温度有关 电离平衡常数不随任何条件而改变
电离平衡常数(K)越小,表示弱电解质电离能力越弱
电离平衡常数(K)与温度无关
不同浓度的同一弱电解质,其电离平衡常数(K)不同
多元弱酸各步电离平衡常数相互关系为:K1<K2<K3
电离平衡常数(K.)与温度无关 H2CO3的电离常数表达式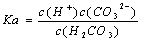 同温下,电离平衡常数越小表示弱电解质电离能力越弱 多元弱酸各步电离平衡常数相互关系为:K123
同温下,电离平衡常数越小表示弱电解质电离能力越弱 多元弱酸各步电离平衡常数相互关系为:K123
碳酸的酸性强于氢硫酸 多元弱酸的酸性主要由第一步电离决定 多元弱酸的各步电离之间无影响 向弱酸溶液中加少量NaOH固体,电离常数不变
各平衡常数的大小与温度有关 若温度升高则各平衡常数一定增大 平衡常数的大小能说明反应(或电离、溶解)进行的程度 平衡常数越大反应(或电离、溶解)程度越大
电离平衡常数能衡量电解质电离的相对强弱 电离平衡常数不随浓度的变化而变化 电离平衡常数与温度有关 电离平衡常数不随任何条件而改变
HNO2的电离平衡常数是③ HNO2的电离平衡常数是① HCN的电离平衡常数是② HF的电离平衡常数是①
电离度越大,电离平衡常数越大; 浓度越稀,电离度越大,电离平衡常数越大; 在相同的温度下电离度可变,而电离平衡常数不变; 多元弱酸的每一步电离平衡常数是相同的

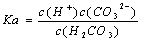 同温下,电离平衡常数越小表示弱电解质电离能力越弱 多元弱酸各步电离平衡常数相互关系为:K1
同温下,电离平衡常数越小表示弱电解质电离能力越弱 多元弱酸各步电离平衡常数相互关系为:K1