你可能感兴趣的试题
该电池不适宜在过高或过低温度下使用 正极反应中有CO2生成 质子通过交换膜从负极区移向正极区 电池总反应为C6H12O6+ 6O2==6CO2 +6H2O
正极反应中有CO2生成 微生物促进了反应中电子的转移 质子通过交换膜从负极区移向正极区 电池总反应为C6H12O6+6O2=6CO2+6H2O
缺氧水解-好氧工艺 固定床微电解工艺 开发和选用新型的混凝剂 生物活性炭工艺
脱硝要考虑为二阶段的生物过程 在适当的条件下,用全混厌氧悬浮生物系统和推流厌氧滤床都能去除废水中90%的硝氯 可完成反硝化作用的微生物,都可将硝酸盐还原到氮原子 选择何种方法处理工业废水的硝酸盐碱主要取决于废水的特性、处理要求以及经济性
A极电极反应式为: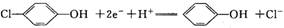 B.极电极反应式为:CH3COO--8e-+4H2O=2HCO3-+9H+ 溶液中的阴离子由A.极向B.极移动 该微生物电池在高温条件下无法正常工作1.
B.极电极反应式为:CH3COO--8e-+4H2O=2HCO3-+9H+ 溶液中的阴离子由A.极向B.极移动 该微生物电池在高温条件下无法正常工作1.
正极反应中有CO2生成 微生物促进了反应中电子的转移[学 质子通过交换膜从负极区移向正极区 电池总反应为C6H12O6+6O2=6CO2+6H2O
正极反应中有CO2生成 微生物促进了反应中电子的转移 质子通过交换膜从负极区移向正极区 电池总反应为C6H12O6+6O2=6CO2+6H2O
正极反应中有CO2生成 微生物促进了反应中电子的转移 质子通过交换膜从负极区移向正极区 电池总反应为C6H12O6+6O2═6CO2+6H2O
正极反应中有CO2生成 微生物促进了反应中电子的转移 质子通过交换膜从负极区移向正极区 电池总反应为C6H12O6+6O2===6CO2+6H2O
X.极为微生物电池的负极 该电池能够在高温下工作 图中离子交换膜应为阴离子交换膜 Y.极电极反应式为:CH3COO--8e-+4H2O=2HCO3-+9H+
正极反应中有CO2生成 微生物促进了反应中电子的转移 质子通过交换膜从负极区移向正极区 电池总反应为C6H12O6+6O2===6CO2+6H2O
还原法处理工业废水是投加还原剂或电解的方法使废水中的污染物质经还原反应转变为无害或少害的新物质 处理含铬废水是利用还原剂将三价铬转化为六价铬 处理含铬废水时还原反应pH值宜控制在7~9 电解法处理含铬废水,六价铬在阳极还原
正极反应中有CO2生成 微生物促进了反应中电子的转移 质子通过交换膜从负极区移向正极区 电池总反应为C6H12O6+6O2===6CO2+6H2O
该电池不适宜在过高或过低温度下使用 正极反应中有CO2生成 质子通过交换膜从负极区移向正极区 电池总反应为C6H12O6+ 6O2==6CO2 +6H2O
正极反应中有CO2生成 微生物促进了反应中电子的转移 质子通过交换膜从负极区移向正极区 电池总反应为C6H12O6+6O2=6CO2+6H2O
高浓度有机工业废水 低浓度工业废水和城市污水 酸性废水 雨水

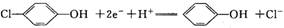 B.极电极反应式为:CH3COO--8e-+4H2O=2HCO3-+9H+ 溶液中的阴离子由A.极向B.极移动 该微生物电池在高温条件下无法正常工作1.
B.极电极反应式为:CH3COO--8e-+4H2O=2HCO3-+9H+ 溶液中的阴离子由A.极向B.极移动 该微生物电池在高温条件下无法正常工作1.