你可能感兴趣的试题
Zn为正极,Ag2O为负极 Zn为负极,Ag2O为正极 原电池工作时,正极区溶液pH值减小 原电池工作时,负极区溶液pH值增大
锌是正极,氧化银是负极 锌发生还原反应,氧化银发生氧化反应 溶液中OH—向正极移动,K+ 、H+向负极移动 随着电极反应的不断进行,电解质溶液中KOH的质量分数不断增大
锌为负极,氧化银为正极
锌为正极,氧化银为负极
原电池工作时,负极区溶液pH增大
该原电池总反应为:Zn+Ag2O+H2O=Zn(OH)2+2Ag
电子由锌经外电路流向氧化银
该电池可实现化学能和电能的相互转化
锌是负极,氧化银是正极
工作时,负极区溶液pH减小,正极区pH增大
电子由锌经外电路流向氧化银 该电池可实现化学能和电能的相互转化 锌是负极,氧化银是正极 工作时,负极区溶液 pH 减小,正极区 pH 增大
原电池放电时,负极上发生反应的物质是Zn 溶液中OH-向正极移动,K+、H+向负极移动 工作时,负极区溶液pH减小,正极区pH增大 负极上发生的反应是Zn+2OH--2e-=Zn(OH)2
在使用过程中,电池负极区溶液pH增大 在使用过程中,电子由Ag2O极经外电路流向Zn极 在使用过程中,Zn电极发生还原反应,Ag2O电极发生氧化反应 外电路中每通过0.2 mol电子,正极的质量理论上减小1.6 g
锌是负极,氧化银是正极 锌发生还原反应,氧化银发生氧化反应 溶液中OH-向正极移动, 、
、 向负极移动 随着电极反应的不断进行,电解质溶液的pH保持不变
向负极移动 随着电极反应的不断进行,电解质溶液的pH保持不变
Zn是正极,Ag2O是负极
Zn是负极,Ag2O是正极
工作时负极区溶液的pH增大
工作时电子由Ag2O极经外电路流向Zn极
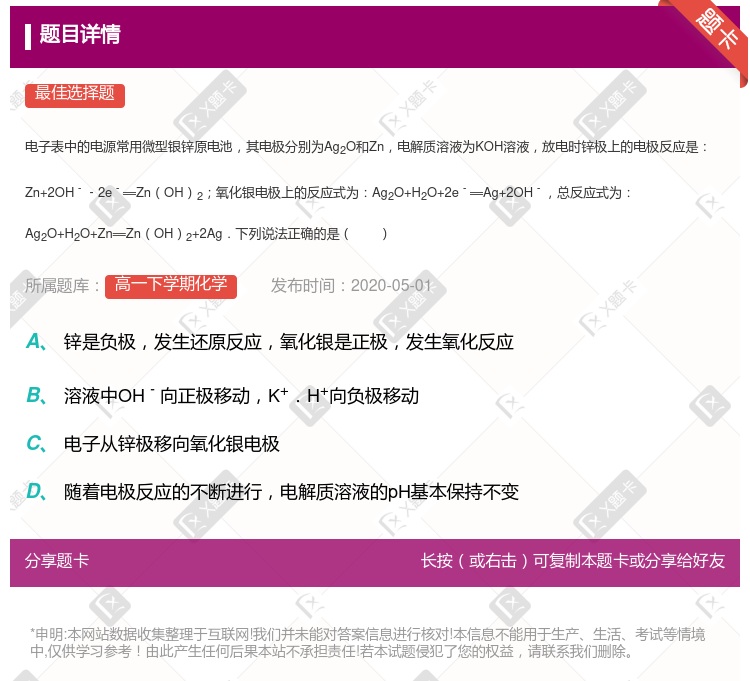
锌是负极,氧化银是正极 锌发生还原反应,氧化银发生氧化反应 溶液中OH-向正极移动,K+、H+向负极移动 随着电极反应的不断进行,电解质溶液的pH保持不变
Zn+2OH--2e-=ZnO+H2O
ZnO+H2O+2e-=Zn+2OH-
Ag2O+2H++2e-=2Ag+H2O
Ag2O+H2O+2e-=2Ag+2OH-
Zn为正极,Ag2O为负极 Zn为负极,Ag2O为正极 原电池工作时,正极区溶液pH值减小 原电池工作时,负极区溶液pH值增大
Zn为正极,Ag2O为负极 Ag2O发生还原反应 原电池工作时,正极区溶液pH值减小 原电池工作时,负极区溶液pH值增大
Zn是正极,Ag2O是负极 负极反应为Zn +2OH--2e-=Zn(OH)2 工作时负极区溶液的pH增大 工作时溶液中K+移向负极
原电池放电时,负极上发生反应的物质是Zn 负极发生的反应是Zn+2OH--2e-===Zn(OH)2 工作时,负极区溶液碱性减弱,正极区溶液碱性增强 溶液中OH-向正极移动,K.+、H.+向负极移动
 、
、 向负极移动 随着电极反应的不断进行,电解质溶液的pH保持不变
向负极移动 随着电极反应的不断进行,电解质溶液的pH保持不变