你可能感兴趣的试题
a为CH4,b为CO2 CO32﹣向正极移动 此电池在常温时也能工作 正极电极反应式为:O2+2CO2+4e﹣=2CO32﹣
0.2mol 0.4mol 0.8mol 0.9mol
通CO的一极是电池的正极 正极反应式为:2CO+2CO32--4e-=4CO2 负极反应式为:O2+2CO2+4e-=2CO32- 该电池工作过程中需不断补充CO和O2,而CO2可循环利用
若浓硝酸体积为 200mL,则其物质的量浓度为 11mol/L NO、NO2、N2O.4 和 NaOH 溶液反应时, NO2、N2O.4 仅作还原剂 生成 0.2 mol NaNO3 和 0.8 mol NaNO2 硝酸在反应中仅体现氧化性
该电池放电时NO3-向石墨Ⅱ电极迁移 石墨Ⅱ附近发生的反应为NO + O2 + e- == NO3- 电池总反应为 4NO2+O2 == 2 N2O5 当外电路通过4mole-时,负极共产生2mol N2O5
放电时,NO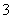 向石墨Ⅱ电极迁移 石墨Ⅱ附近发生的反应为NO+O2+e-===NO
向石墨Ⅱ电极迁移 石墨Ⅱ附近发生的反应为NO+O2+e-===NO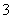 该电池总反应式为4NO2+O2===2N2O5 当外电路通过4 mol e-时,负极上共产生2mol N2O5
该电池总反应式为4NO2+O2===2N2O5 当外电路通过4 mol e-时,负极上共产生2mol N2O5
通CO的一极是电池的正极, 该电池工作过程中需不断补充CO和O2,CO2可循环利用 负极反应式:O2+2CO2+4e-==2CO32- 该电池工作过程中有蓝色火焰产生
通CO的一极是电池的正极, 该电池工作过程中需不断补充CO和O2,CO2可循环利用 负极反应式:O2+2CO2+4e-==2CO32- 该电池工作过程中有蓝色火焰产生
a为CH4,b为CO2 CO 向正极移动 此电池在常温时也能工作 正极电极反应式为:O2+2CO2+4e-===2CO
向正极移动 此电池在常温时也能工作 正极电极反应式为:O2+2CO2+4e-===2CO
正极反应为4OH--4e- O2↑+2H2O 放电时, CO32-向负极移动 电池供应1 mol水蒸气,转移的电子的物质的量为4 mol 放电时CO32-向正极移动
O2↑+2H2O 放电时, CO32-向负极移动 电池供应1 mol水蒸气,转移的电子的物质的量为4 mol 放电时CO32-向正极移动
该电池的a、b极材料可以是同种金属 该电池是一种高效、环境友好的发电装置 外电路中电子由电极b通过导线流向电极a 该电池的总反应:2H2 + O2 = 2H2O
b电极是正极 a电极的电极反应为: O2 +2 H2O+ 4e- = 4OH- 氢氧燃料电池中的电子是从a电极经外电路流向b电极 氢氧燃料电池是一种不需要将还原剂和氧化剂全部储藏在电池内的新型发电装置 
通CO的一极是电池的正极 负极电极反应是:O2+2CO2+4e―=2CO32― 熔融盐中CO32―的物质的量在工作时保持不变 正极发生氧化反应
碱性燃料电池 磷酸燃料电池 熔融碳酸盐燃料电池 固态氧化物燃料电池 质子交换膜燃料电池

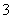 向石墨Ⅱ电极迁移 石墨Ⅱ附近发生的反应为NO+O2+e-===NO
向石墨Ⅱ电极迁移 石墨Ⅱ附近发生的反应为NO+O2+e-===NO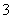 该电池总反应式为4NO2+O2===2N2O5 当外电路通过4 mol e-时,负极上共产生2mol N2O5
该电池总反应式为4NO2+O2===2N2O5 当外电路通过4 mol e-时,负极上共产生2mol N2O5
 向正极移动 此电池在常温时也能工作 正极电极反应式为:O2+2CO2+4e-===2CO
向正极移动 此电池在常温时也能工作 正极电极反应式为:O2+2CO2+4e-===2CO
 O2↑+2H2O 放电时, CO32-向负极移动 电池供应1 mol水蒸气,转移的电子的物质的量为4 mol 放电时CO32-向正极移动
O2↑+2H2O 放电时, CO32-向负极移动 电池供应1 mol水蒸气,转移的电子的物质的量为4 mol 放电时CO32-向正极移动
