

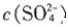 的BaSO4溶液中加入BaSO4固体,
的BaSO4溶液中加入BaSO4固体,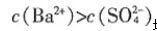 增大 向该饱和溶液中加入Ba(NO3)2固体,则BaSO4的溶度积常数增大 向该饱和溶液中加入Na2SO4固体,则该溶液中
增大 向该饱和溶液中加入Ba(NO3)2固体,则BaSO4的溶度积常数增大 向该饱和溶液中加入Na2SO4固体,则该溶液中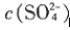 向该饱和溶液中加入BaCl2固体,则该溶液中
向该饱和溶液中加入BaCl2固体,则该溶液中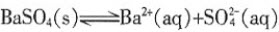 减小
减小
 (aq)===BaSO4(s) ΔH=-2.92 kJ·mol-1 Ba2+(aq)+SO
(aq)===BaSO4(s) ΔH=-2.92 kJ·mol-1 Ba2+(aq)+SO (aq)===BaSO4(s) ΔH=-18 kJ·mol-1 Ba2+(aq)+SO
(aq)===BaSO4(s) ΔH=-18 kJ·mol-1 Ba2+(aq)+SO (aq)===BaSO4(s) ΔH=-73 kJ·mol-1 Ba2+(aq)+SO
(aq)===BaSO4(s) ΔH=-73 kJ·mol-1 Ba2+(aq)+SO (aq)===BaSO4(s) ΔH=-0.72 kJ·mol-1
(aq)===BaSO4(s) ΔH=-0.72 kJ·mol-1


 (aq)===BaSO4(s) ΔH=-2.92 kJ·mol-1 Ba2+(aq)+SO
(aq)===BaSO4(s) ΔH=-2.92 kJ·mol-1 Ba2+(aq)+SO (aq)===BaSO4(s) ΔH=-18 kJ·mol-1 Ba2+(aq)+SO
(aq)===BaSO4(s) ΔH=-18 kJ·mol-1 Ba2+(aq)+SO (aq)===BaSO4(s) ΔH=-73 kJ·mol-1 Ba2+(aq)+SO
(aq)===BaSO4(s) ΔH=-73 kJ·mol-1 Ba2+(aq)+SO (aq)===BaSO4(s) ΔH=-0.72 kJ·mol-
(aq)===BaSO4(s) ΔH=-0.72 kJ·mol-