你可能感兴趣的试题
R.可以是Zn 因生成气体,反应后溶液质量减小 该反应是化合反应 R.若是Fe,则反应前后溶液颜色有变化
化学反应速率只能用反应物浓度的减少来表示 同一化学反应,相同条件下用不同物质表示反应速率,其数值可能不同,但表示意义相同 化学平衡状态指的是反应物和生成物浓度相等时的状态 将稀盐酸换成浓硫酸或浓硝酸,可以使反应Fe(s)+2HCl(aq)===FeCl2(aq)+H2(g)生成H2速率增大
2R+3H2SO4=R2(SO4)3+3H2↑ 4R+3O2 2R2O3 R+2HCl=R2Cl2+H2↑ 2R+6HCl=2RCl3+3H2↑
2R2O3 R+2HCl=R2Cl2+H2↑ 2R+6HCl=2RCl3+3H2↑
Zn+2HCl =ZnCl 2+ H2↑ H 2SO4+NaCl =NaHSO4+HCl Fe2O3+6HCl =2FeCl3+3H2O NaCl +AgNO 3=AgCl ↓+ NaNO3
该反应是置换反应 R.可能是金属Fe Cu的活动性比R.强 该反应前后R.的化合价发生了改变
用HCl和CaCl2表示的反应速率数据不同,但所表示的意义相同 不能用CaCO3的浓度变化来表示反应速率,但可用水来表示 用H2O和CO2表示的化学反应速率相同 用CaCl2浓度的减小表示其反应速率
用HCl和CaCl2表示的反应速率数值不同,但所表示的意义相同 不能用CaCO3浓度的变化来表示反应速率,但可用水来表示 用H2O和CO2表示的化学反应速率相同 用CaCl2浓度的减少来表示其反应速率
将木炭粉成粉末状可以加快化学反应速率 升高温度可以加快化学反应速率 增加压强可以加快化学反应速率 增加木炭的量可以加快化学反应速率
该反应是置换反应 金属R.可能是铝 金属R.活动性比Cu强 该反应前后R.的化合价发生了改变
H2CO3===H2O+CO2↑ NH3+HCl===NH4Cl 2HI+Cl2===2HCl+I2 ↓ NaOH+HCl===NaCl+H2O
R+MgSO4=== RSO4+Mg R+CuSO4=== RSO4+Cu R+H2SO4=== RSO4+H2↑ 2Al+3RSO4=== Al2(SO4)3+3R
2R + 3H2SO4 = R2(SO4)3 + 3H2↑ 4R + 3O2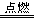 2R2O3 R + 2HCl = RCl2 + H2↑ 2R + 6HCl = 2RCl3 + 3H2↑
2R2O3 R + 2HCl = RCl2 + H2↑ 2R + 6HCl = 2RCl3 + 3H2↑
1 mol H2(g)和1 mol Cl2(g)具有的总能量大于2 mol HCl(g)具有的总能量 该反应的△H. > 0 通常情况下,H 2(g)和Cl2(g)混合容易直接生成HCl(g) 生成的HCl溶于水会发生电离,即HCl=H++Cl-,由此判断,HCl中存在离子键
Fe+HCl=FeCl2+H2↑ Fe+2HCl=FeCl2+H2↑ Fe+2HCl=FeC13+H2↑ Fe+2HCl=FeCl+H2↑
其他条件不变,适当增加盐酸的浓度将加快化学反应速率 其他条件不变,适当增加CaCO3的用量将加快化学反应速率 反应过程中,化学反应速率将先增大后减小 一定条件下反应速率改变,△H<0不变
1/2H2(g)+ 1/2Cl2(g)=HCl(g);△H=-91.5 kJ・mol-1 H2(g)+ Cl2(g)=2HCl(g); △H=-183 kJ・mol-1 1/2H2(g)+ 1/2Cl2(g)=HCl(g);△H=+91.5 kJ・mol-1 2HCl(g)= H2(g)+ Cl2(g); △H=+183kJ・mol-1
2R+3H2SO4=R2(SO4)3+3H2↑ 4R+3O2 2R2O3 R+2HCl=R2Cl2+H2↑ 2R+6HCl=2RCl3+3H2↑
2R2O3 R+2HCl=R2Cl2+H2↑ 2R+6HCl=2RCl3+3H2↑
R+MgSO4===RSO4+Mg R+CuSO4===RSO4+Cu R+H2SO4===RSO4+H2↑ 2Al+3RSO4===Al2(SO4)3+3R
R+MgSO4=== RSO4+Mg R+CuSO4=== RSO4+Cu R+H2SO4=== RSO4+H2↑ 2A1+3RSO4=== Al2(SO4)3+3R

 2R2O3 R+2HCl=R2Cl2+H2↑ 2R+6HCl=2RCl3+3H2↑
2R2O3 R+2HCl=R2Cl2+H2↑ 2R+6HCl=2RCl3+3H2↑
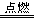 2R2O3 R + 2HCl = RCl2 + H2↑ 2R + 6HCl = 2RCl3 + 3H2↑
2R2O3 R + 2HCl = RCl2 + H2↑ 2R + 6HCl = 2RCl3 + 3H2↑
 2R2O3 R+2HCl=R2Cl2+H2↑ 2R+6HCl=2RCl3+3H2↑
2R2O3 R+2HCl=R2Cl2+H2↑ 2R+6HCl=2RCl3+3H2↑