你可能感兴趣的试题
该温度下醋酸的电离平衡常数约为1×10-5mol·L-1 图中V1 > 20mL,且a点对应的溶液中:c (Na+)+ c (H+) = c (OH-)+ c (CH3COO-) 图中V1 < 20mL,且a点对应的溶液中:c (CH3COOH) + c (CH3COO-) +) 当加入Na OH溶液的体积为20mL时,溶液中:c (CH3COOH) + c (H+) > c (OH-)
常温下,0.1 mol·L-1的NaHSO3溶液(呈酸性)中:c(Na+)>c(HSO )>c(SO
)>c(SO )>c(H2SO3) 常温下,pH相等的CH3COONa、NaOH和Na2CO3三种溶液: c(NaOH)<c(Na2CO3)<c(CH3COONa) 常温下,0.1 mol/L Na2CO3溶液:c(OH-)=c(HCO3-)+c(H+)+2c(H2CO3) 常温下,0.1 mol·L-1的Na2CO3溶液中:2c(Na+)=c(CO
)>c(H2SO3) 常温下,pH相等的CH3COONa、NaOH和Na2CO3三种溶液: c(NaOH)<c(Na2CO3)<c(CH3COONa) 常温下,0.1 mol/L Na2CO3溶液:c(OH-)=c(HCO3-)+c(H+)+2c(H2CO3) 常温下,0.1 mol·L-1的Na2CO3溶液中:2c(Na+)=c(CO )+ c(HCO
)+ c(HCO )+c(H2CO3)
)+c(H2CO3)
图①表示25℃时,和0.1mol·L-1盐酸滴定20mL 0.1mol·L-1NaOH溶液 图②表示常温下,等量锌粉与足量的等体积等浓度的盐酸反应 图③表示向CaCl2和盐酸的混合溶液中滴加Na2CO3溶液 图④表示向盐酸和醋酸混合溶液中滴入氨水
相同温度下,中和pH=1的盐酸和醋酸各20.0 mL,需要0.100 mol·L-1 NaOH溶液都是20.0 mL 0.1 mol·L-1 Na2CO3溶液中加入少量NaOH固体后振荡,c(Na+)和c(CO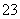 )都增大 常温下,向AgCl悬浊液中加入少量NaCl固体后振荡,K.sp(AgCl)增大 相同浓度的CH3COOH和CH3COONa溶液等体积混合后,c(CH3COO-)+c(CH3COOH)=c(Na+)
)都增大 常温下,向AgCl悬浊液中加入少量NaCl固体后振荡,K.sp(AgCl)增大 相同浓度的CH3COOH和CH3COONa溶液等体积混合后,c(CH3COO-)+c(CH3COOH)=c(Na+)
常温下,20mL中含X.、Y.各0.003mol的溶液 常温下,100mL中含X.、Y.各0.005mol的溶液 常温下,0.1mol/L.的X.、Y.溶液各l0mL相混合 标准状况下,0.1mol/L.的X.、Y.溶液各l0mL相混合
pH=2的HA溶液与pH=12的MOH溶液任意比混合: c(H+) + c(M+) === c(OH-) + c(A-) pH相等的CH3COONa、NaOH和Na2CO3三种溶液: c(NaOH)<c(CH3CO ONa)<c(Na2CO3) 物质的量浓度相等CH3COOH和CH3COONa溶液等体积混合: c(CH3COO-) +2c(OH-) === c(H+) + c(CH3COOH) 0.1mol•L-1的NaHA溶液,其pH=4:c(HA-)>c(H+)>c(H2A)>c(A2-)
常温下,在pH=8的NaA溶液中:c(Na+)-c(A-)=9.9×10-7 mol·L-1 由10 mL 0.1 mol·L-1的CH3COOH溶液与10 mL 0.1 mol·L-1的NaOH溶液混合,离子浓度大小的顺序:c(Na+)>c(OH-)>c(CH3COO-)>c(H+) 室温下,由pH=1的CH3COOH溶液与pH=13的NaOH溶液等体积混合,浓度大小的顺序:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) 常温下,0.1 mol·L-1 pH=8的NaHB溶液中:c(B2-)>c(H2B.)
0.10 mol·L-1的醋酸钠溶液20mL与0.10 mol·L-1盐酸10mL混合后溶液显酸性: c (CH3COO-)>c (Cl-)>c (H+)>c (CH3COOH) pH=7的醋酸钠和醋酸混合液中:c(Na+)= c(CH3COO-)= c (H+)=c(OH-) 若0.10 mol·L-1的醋酸的pH=a,0.010 mol·L-1的醋酸的pH=b,则a+1>b 已知酸性HF>CH3COOH,pH相等的NaF与CH3COOK溶液中: [c(Na+)-c(F-)]< [c(K+)-c(CH3COO-)]
pH相等的①NH4Cl、②(NH4)2SO4、③NH4HSO4的溶液中,c(NH4+)大小:①=②>③ 常温下,在10mL pH=12的氢氧化钠溶液中加入pH=2的HA至pH刚好等于7,所得溶液体积V.(总)≤20mL 向1.00L 0.3mol·L-1的NaOH溶液中缓慢通入CO2气体至溶液增重8.8g,所得溶液中:3c(Na+)=2[c(HCO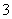 )+c(CO
)+c(CO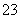 )+c(H2CO3)] 浓度均为0.1mol·L-1的CH3COOH和CH3COONa溶液等体积混合: c(CH3COO-)-c(CH3COOH)=c(H+)-c(OH-)
)+c(H2CO3)] 浓度均为0.1mol·L-1的CH3COOH和CH3COONa溶液等体积混合: c(CH3COO-)-c(CH3COOH)=c(H+)-c(OH-)
150 mL 1 mol/L盐酸 20 mL 18.4 mol/L硫酸 50 mL 3 mol/L盐酸 250 mL 2 mol/L硫酸
0.1mol/L的醋酸钠溶液20mL与0.1mol/L盐酸10mL混合后溶液显酸性 c (CH3COO-)>c (Cl-)>c (H+)>c (CH3COOH) pH=7的醋酸钠和醋酸混合液中:c(Na+)= c(CH3COO-) 0.1mol/L的醋酸的pH=a,0.01mol/L的醋酸的pH=b,则a+1>b 已知酸性HF>CH3COOH,pH相等的NaF与CH3COOK溶液中, [c(Na+)-c(F.一)]<[c(K+)-c(CH3COO一)]
a点表示的溶液中c(CH3COO-)略小于10-3mol/L b点表示的溶液中c(CH3COO-)>c(Na+) c点表示CH3COOH和NaOH恰好反应完全 b、d点表示的溶液中 均为Ka
均为Ka
常温下同浓度的强酸、强碱等体积混合后由水电离出的c(H+) =10-7mol·L-l 常温下pH =2的盐酸和pH =12的氨水等体积混合后c(C1-)+c(H+)=c(NH4+)+c(OH-) 常温下0.1 mol.L.-1的Na2A溶液的pH=10,则该溶液中由水电离的c(OH-)= 10 -10 mol.L.-l 常温下向10 mL0.1 mol.L.-1的CH3COOH溶液中滴加相同浓度的氨水,在滴加过程中, 将减小
将减小
0.1 mol·L-1CH3COOH溶液加水稀释,溶液中所有离子浓度均减小 常温下,在由水电离出的c(OH-)=1×10-12mol•L-1的溶液中,Al3+可能大量存在 常温下,向AgCl悬浊液中加入少量NaCl固体后振荡,Ksp(AgCl)增大 常温下,相同浓度的CH3COONa溶液与Na2CO3溶液相比,Na2CO3溶液的pH小
20mL0.3 mol·L-1Na2CO3 10mL0.4 mol·L-1Na2CO3 25mL0.4 mol·L-1Na2CO3 15mL0.5 mol·L-1Na2CO3
②>④>③>① ①>②>④>③ ①>②>③>④ ③>②>④>①
+B⇌AB来说,常温下按以下情况进行反应:
①20mL溶液中含A. 各0.01mol ②50mL溶液中含A.B.各0.05mol
③0.1 mol•L.-1的A.B.溶液各10mL ④0.5 mol•L.-1的A.B.溶液各50mL
四者反应速率大小关系是( )
A.②>①>④>③ B.④>③>②>① ①>②>④>③ ①>②>③>④
0.1 mol/L.的醋酸钠溶液20mL与0.1 mol/L.盐酸10 mL混合后溶液显酸性 c(Ac一)>c(Cl一)>c(H+)>c(HAc) pH>7的醋酸钠和醋酸混合液中:c(Na+)=c(CH3COO一) 0.1mol/L.的醋酸的7pH=a,0.01mol/L.的醋酸的pH=b,则a+1>b 已知酸性HF>CH3COOH,pH相等的NaF与CH3COOK溶液中, [c(Na+)一c(F )]<[c(K+)一c(CH3COO一)]
)]<[c(K+)一c(CH3COO一)]
c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(OH-) c(Cl-)>c(CH3COO-)>c(CH3COOH)>c(H+) c(CH3COO-)=c(Cl-)=c(CH3COOH)>c(OH-) c(CH3COOH)>c(Cl-)>c(CH3COO-)>c(H+)


 )>c(SO
)>c(SO )>c(H2SO3) 常温下,pH相等的CH3COONa、NaOH和Na2CO3三种溶液: c(NaOH)<c(Na2CO3)<c(CH3COONa) 常温下,0.1 mol/L Na2CO3溶液:c(OH-)=c(HCO3-)+c(H+)+2c(H2CO3) 常温下,0.1 mol·L-1的Na2CO3溶液中:2c(Na+)=c(CO
)>c(H2SO3) 常温下,pH相等的CH3COONa、NaOH和Na2CO3三种溶液: c(NaOH)<c(Na2CO3)<c(CH3COONa) 常温下,0.1 mol/L Na2CO3溶液:c(OH-)=c(HCO3-)+c(H+)+2c(H2CO3) 常温下,0.1 mol·L-1的Na2CO3溶液中:2c(Na+)=c(CO )+ c(HCO
)+ c(HCO )+c(H2CO3)
)+c(H2CO3)
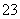 )都增大 常温下,向AgCl悬浊液中加入少量NaCl固体后振荡,K.sp(AgCl)增大 相同浓度的CH3COOH和CH3COONa溶液等体积混合后,c(CH3COO-)+c(CH3COOH)=c(Na+)
)都增大 常温下,向AgCl悬浊液中加入少量NaCl固体后振荡,K.sp(AgCl)增大 相同浓度的CH3COOH和CH3COONa溶液等体积混合后,c(CH3COO-)+c(CH3COOH)=c(Na+)
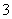 )+c(CO
)+c(CO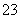 )+c(H2CO3)] 浓度均为0.1mol·L-1的CH3COOH和CH3COONa溶液等体积混合: c(CH3COO-)-c(CH3COOH)=c(H+)-c(OH-)
)+c(H2CO3)] 浓度均为0.1mol·L-1的CH3COOH和CH3COONa溶液等体积混合: c(CH3COO-)-c(CH3COOH)=c(H+)-c(OH-)
 均为Ka
均为Ka
 将减小
将减小
 )]<[c(K+)一c(CH3COO一)]
)]<[c(K+)一c(CH3COO一)]