你可能感兴趣的试题
充电时Li+从阳极区移向阴极区 充电时阴极反应为LiOH+e-═Li+OH- 放电时负极上I- 被氧化 放电时正极反应为O2+2H2O+4Li++4e-═4LiOH
此电池的正极为Ni2O3、负极为Al,电池中的凝胶呈碱性。 电池放电时,负极反应为Al + 3OH- - 3e-= Al(OH)3 电池充电过程中,阴极附近溶液的pH升高 电池充电时,阴极反应为2Ni(OH)2 + 2OH- - 2e- = Ni2O3 + 3H2O
充电时阴极发生氧化反应 充电时将碳电极与电源的正极相连 放电时碳电极反应为原电池的负极 放电时镍电极反应为Ni(OH)2-e-+OH-=NiO(OH)+H2O
放电时,铝为负极,石墨为正极 放电时的负极反应为:Al-3e-+7AlCl4-===4Al2Cl7- 充电时的阳极反应为:Cx+ AlCl4--e-===CxAlCl4 放电时,有机阳离子向铝电极方向移动
放电时负极反应为:Zn — 2e— + 2OH— == Zn(OH)2 充电时阳极反应为:Fe(OH)3 — 3e— + 5OH— == FeO42— + 4H2O 放电时每转移3moL电子,正极有1 mol K2FeO4被氧化 放电时正极附近溶液的碱性增强
放电时K.+移向碳电极 放电时电池负极的电极反应为H2-2e-= 2H+ 充电时镍电极的电极反应为 Ni(OH)2 + OH——e-= NiO(OH) + H2O 该电池充电时将碳电极与电源的正极相连, 发生氧化反应
放电时,铝为负极、石墨为正极 放电时的负极反应为:Al –3e- + 7AlCl4– = 4Al2Cl7– 充电时的阳极反应为:Cn + AlCl4––e- = CnAlCl4 放电时,有机阳离子向铝电极方向移动
放电时负极上I.- 被氧化 充电时Li+从阳极区移向阴极区 充电时阴极反应为LiOH+e-==Li+OH- 放电时正极反应为O2+2H2O+4Li++4e-==4LiOH
放电时,铝为负极、石墨为正极 放电时的负极反应为:Al –3e- + 7AlCl4– =4Al2Cl7– 充电时的阳极反应为:Cn + AlCl4– – e- =CnAlCl4 放电时,有机阳离子向铝电极方向移动
充电时阳极反应为: 放电时负极反应为:
放电时负极反应为: 放电时每转移
放电时每转移 电子,正极有
电子,正极有 被氧化 放电时正极附近溶液的碱性增强
被氧化 放电时正极附近溶液的碱性增强
放电时,电极a发生还原反应 放电时,电解质中Na+由电极a移向电极b 电池充电时的总反应为2Na+NiCl2=2NaCl+Ni 可将装置中的固体电解质改为NaCl溶液
充电时的阳极反应为:Cn+AlCl 4– – e- =CnAlCl 4 放电时,铝为负极、石墨为正极 放电时,有机阳离子向铝电极方向移动 放电时的负极反应为:Al–3e-+7AlCl 4– = 4Al2Cl 7– 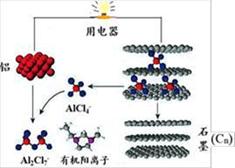

 放电时负极反应为:
放电时负极反应为: 放电时每转移
放电时每转移 电子,正极有
电子,正极有 被氧化 放电时正极附近溶液的碱性增强
被氧化 放电时正极附近溶液的碱性增强
