你可能感兴趣的试题
放电时,负极的电极反应式:Li-e- Li+ 充电时,Li0.85NiO2既发生氧化反应又发生还原反应 该电池不能用水溶液作为电解质 放电过程中Li+向负极移动
Li+ 充电时,Li0.85NiO2既发生氧化反应又发生还原反应 该电池不能用水溶液作为电解质 放电过程中Li+向负极移动
放电时,负极的电极反应式:Li-e-===Li+ 充电时,Li0.85NiO2既发生氧化反应又发生还原反应 该电池不能用水溶液作为电解质 放电过程中Li+向负极移动
放电时,负极的电极反应式:Li-e- = Li+ 充电时,Li0.85NiO2既发生氧化反应又发生还原反应 该电池不能用水溶液作为电解质 放电过程中Li+向负极移动
放电时电池内部Li+向负极移动 该电池不能选用水做溶剂的电解质 放电时,正极的电极反应式:0.45Li++Li0。55CoO2+0.45e- LiCoO2 充电时,外接电源的正极与电池上标注“+”的电极连接
该电池可以用NaOH溶液为电解质溶液 放电时电池正极的电极反应式为Fe2O3+6Li++6e-=3Li2O+2Fe 充电时,Fe作为阴极,电池不被磁铁吸引 磁铁的主要成分是Fe3O4,其既可吸引铁,也可吸引Fe2O3
充电时,电池的阳极反应为LiC6 — e— = Li+ + C6 放电时,电池的正极反应为 CoO2 +Li++ e— = LiCoO2 乙酸、乙醇等含活泼氢的有机物可做该锂离子电池的电解质 该锂离子电池的比能量(消耗单位质量电极所释放的电量)比铅蓄电池低
锂离子电池充电时电池反应为 电池反应中,锂、锌、银、铅各失去1mol电子,金属锂所消耗的质量最小 锂离子电池放电时电池内部Li+向负极移动 锂离子电池充电时阴极反应为:
电池反应中,锂、锌、银、铅各失去1mol电子,金属锂所消耗的质量最小 锂离子电池放电时电池内部Li+向负极移动 锂离子电池充电时阴极反应为:
放电时,负极的电极反应式: 充电时,Li0.85NiO2既发生氧化反应又发生还原反应 该电池不能用水溶液作为电解质 放电过程中Li+向负极移动
充电时,Li0.85NiO2既发生氧化反应又发生还原反应 该电池不能用水溶液作为电解质 放电过程中Li+向负极移动
放电时,负极的电极反应式:Li-e-===Li+ 充电时,Li0.85NiO2既发生氧化反应又发生还原反应 该电池不能用水溶液作为电解质溶液 放电过程中Li+向负极移动
)放电时,负极的电极反应式为:LI++e— = Li; ( )充电时,Li发生氧化反应 ( )该电池不能用水溶液作为电解质; ( )放电过程中Li+ 向负极移动
锂离子电池充电时电池反应为LiMO2+C6Li1-x===C6Li+Li1-xMO2 电池反应中,锂、锌、银、铅各失去1 mol 电子,金属锂所消耗的质量最大 锂离子电池放电时电池内部Li+向负极移动 锂离子电池充电时阴极反应为C6Li1-x+xLi+-xe-===C6Li
锂离子电池充电时电池反应为C6Li+Li1-xMO2=LiMO2+C6Li1-x 电池反应中,锂、锌、银、铅各失去1mol电子,金属锂所消耗的质量最小 锂离子电池放电时电池内部Li+向负极移动 锂离子电池充电时阴极反应为C6Li1-x+xLi++x e-=C6Li
锂离子电池充电时电池反应为C6Li+Li1-xMO2===LiMO2+C6Li1-x 电池反应中,锂、锌、银、铅各失去1mol电子,金属锂所消耗的质量最大 锂离子电池放电时电池内部Li+向正极移动 锂离子电池充电时阴极反应为C6Li1-x+xLi+-x e-=C6Li
放电时,负极的电极反应式:Li-e-=Li+ 充电时,Li0.85NiO2既发生氧化反应又发生还原反应 该电池不能用水溶液作为电解质 放电过程中Li+向负极移动
放电时电池内部Li+向负极移动 该电池不能选用水做溶剂的电解质 放电时,正极的电极反应式:0.45Li++Li0。55CoO2+0.45e- LiCoO2 充电时,外接电源的正极与电池上标注“+”的电极连接
放电时,Li+通过电解质溶液由负极向正极移动 充电时,有机阴离子向a极移动 充电时a电极反应为Fe3O.4 + 8e- + 8Li+ =3Fe+ 4Li2O. 若用该电池电解稀硫酸共产生3.36L气体(标准状况下),电池负极质量 减小1.4g
锂离子电池充电时电池反应为C6Li+Li1-xMO2===LiMO2+C6Li1-x 电池反应中,锂、锌、银、铅各失去1mol电子,金属锂所消耗的质量最小 锂离子电池放电时电池内部Li+向负极移动 锂离子电池充电时阴极反应为C6Li1-x+xLi++x e-===C6Li
放电时,负极的电极反应式:Li-e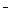 =Li
=Li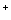 充电时,Li
充电时,Li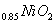 既发生氧化反应又发生还原反应 该电池不能用水溶液作为电解质 放电过程中Li
既发生氧化反应又发生还原反应 该电池不能用水溶液作为电解质 放电过程中Li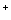 向负极移动
向负极移动
放电时,正极的电极反应式为Fe2O3+6li++6e﹣=2Fe+3Li2O
该电池可以用水溶液做电解质溶液
放电时,Fe作电池的负极,Fe2O3作电池的正极
充电时,电池被磁铁吸引
放电时,负极的电极反应式为Li﹣e﹣=Li+
放电时,电子通过电解质从Li流向Fe2O3
充电时,Fe做阳极,电池逐渐摆脱磁铁吸引
充电时,阳极的电极反应式为2Fe+3Li2O﹣6e﹣=Fe2O3+6Li+

 Li+ 充电时,Li0.85NiO2既发生氧化反应又发生还原反应 该电池不能用水溶液作为电解质 放电过程中Li+向负极移动
Li+ 充电时,Li0.85NiO2既发生氧化反应又发生还原反应 该电池不能用水溶液作为电解质 放电过程中Li+向负极移动
 电池反应中,锂、锌、银、铅各失去1mol电子,金属锂所消耗的质量最小 锂离子电池放电时电池内部Li+向负极移动 锂离子电池充电时阴极反应为:
电池反应中,锂、锌、银、铅各失去1mol电子,金属锂所消耗的质量最小 锂离子电池放电时电池内部Li+向负极移动 锂离子电池充电时阴极反应为:
 充电时,Li0.85NiO2既发生氧化反应又发生还原反应 该电池不能用水溶液作为电解质 放电过程中Li+向负极移动
充电时,Li0.85NiO2既发生氧化反应又发生还原反应 该电池不能用水溶液作为电解质 放电过程中Li+向负极移动
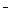 =Li
=Li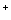 充电时,Li
充电时,Li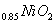 既发生氧化反应又发生还原反应 该电池不能用水溶液作为电解质 放电过程中Li
既发生氧化反应又发生还原反应 该电池不能用水溶液作为电解质 放电过程中Li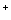 向负极移动
向负极移动