你可能感兴趣的试题
Fe(NO3)3、Cu(NO3)2、HNO3混合溶液中逐渐加入铁粉 Na2CO3、NaHCO3溶液中逐滴加入HCl KAl(SO4)2溶液中逐滴加入Ba(OH)2 溶液 NaAlO2溶液中逐渐通入CO2
D. A. 含0.01 mol KOH和0.01 mol Ca(OH)2的混合溶液中缓慢通入CO2 B. NaHSO4溶液中逐滴加入Ba(OH)2溶液 C. KAl(SO4)2溶液中逐滴加入Ba(OH)2溶液 NaAlO2溶液中逐滴加入盐酸
含0.01 mol KOH和0.01 mol Ca(OH)2的混合溶液中缓慢通入CO2  NaHSO4溶液中逐滴加入Ba(OH)2溶液
NaHSO4溶液中逐滴加入Ba(OH)2溶液 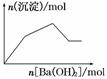 KAl(SO4)2溶液中逐滴加入Ba(OH)2溶液
KAl(SO4)2溶液中逐滴加入Ba(OH)2溶液 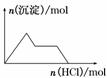 NaAlO2溶液中逐滴加入盐酸
NaAlO2溶液中逐滴加入盐酸
pH = a的氨水溶液,稀释10倍后,其pH = b,则a = b + 1 向NaAlO2溶液中滴加NaHCO3溶液,有沉淀和气体生成 在Na2C2O4稀溶液中,c(OH-) = c(H+) + c(HC2O4—) + 2c(H2C2O4) 0.1 mol/L Na2CO3溶液与0.1 mol/L NaHCO3溶液等体积混合: 3c(Na+) = 2[c(CO32—) + c(HCO3—) + c(H2CO3) ]
原混合溶液中的CO32-与AlO2-的物质的量之比为1:2 V1:V2=1:5 M.点时生成的CO2为0.05mol a曲线表示的离子方程式为:AlO2-+H++H2O=Al(OH)3↓
含0.01mol KOH和0.01mol Ca(OH)2 的混合溶液中缓慢通入CO2 NaHSO4溶液中逐滴加入Ba(OH)2溶液 KAl(SO4)2溶液中逐滴加入Ba(OH)2溶液 NaAlO2溶液中逐滴加入盐酸
原混合溶液中的CO32-与AlO2-的物质的量之比为1∶2 V1∶V2=l∶5 M点时生成的CO2为0.05 mol a曲线表示的离子方程式为AlO2-+H++H2O==Al(OH)3↓
三氯化铝溶液中加入过量氨水:Al3++4NH3·H2O==4NH4++AlO2—+2H2O 4 mol/L的NaAlO2溶液和7 mol/L的HCl溶液等体积互相均匀混合: 4AlO2—+7H++H2O = 3Al(OH)3↓+Al3+ 在Mn2+的溶液中加入HNO3再加入PbO2,得紫红色溶液: 5PbO2+2Mn2++4H+ = 5Pb2++2MnO4—+2H2O 将数滴0.1 mol/L的Na2CO3溶液缓缓滴入0.1 mol/L 25 mL盐酸溶液中:2H++ CO32— =CO2↑+ H2O
D. A. 含0.01 mol KOH和0.01 mol Ca(OH)2的混合溶液中缓慢通入CO2 B. NaHSO4溶液中逐滴加入Ba(OH)2溶液 C. KAl(SO4)2溶液中逐滴加入Ba(OH)2溶液 NaAlO2溶液中逐滴加入盐酸
含0.0l mol KOH和0.01 molCa(OH)2的混合溶液中缓慢通入CO2 NaHSO4溶液中逐滴加入Ba(OH)2溶液 KAl(SO4)2溶液中逐滴加入Ba(OH)2溶液 NaAlO2溶液中逐滴加入盐酸
a曲线表示的离子方程式为:AlO2﹣+H++H2O═Al(OH)3↓ b和c曲线表示的离子反应是相同的 M.点时,溶液中沉淀的质量为3.9g 原混合溶液中的CO32﹣与AlO2﹣的物质的量之比为1:2
向含0.01mol KOH和0.01mol Ca(OH)2的混合溶液中缓慢通入CO2至过量 向NaHSO4溶液中逐滴加入Ba(OH)2溶液至过量 向KAl(SO4)2溶液中逐滴加入Ba(OH)2溶液至过量 向NaAlO2溶液中逐滴加入盐酸至过量 
D.A. 含0.01 mol KOH和0.01 mol Ca(OH)2的混合溶液中缓慢通入CO2B. NaHSO4溶液中逐滴加入Ba(OH)2溶液C. KAl(SO4)2溶液中逐滴加入Ba(OH)2溶液 NaAlO2溶液中逐滴加入盐酸

 NaHSO4溶液中逐滴加入Ba(OH)2溶液
NaHSO4溶液中逐滴加入Ba(OH)2溶液  KAl(SO4)2溶液中逐滴加入Ba(OH)2溶液
KAl(SO4)2溶液中逐滴加入Ba(OH)2溶液  NaAlO2溶液中逐滴加入盐酸
NaAlO2溶液中逐滴加入盐酸
