你可能感兴趣的试题
两溶液的导电能力相同 分别稀释100倍后,溶液pH相同 盐酸中水的电离程度比醋酸中的小 分别与足量Zn反应时,醋酸中生成的n(H2)较多
两溶液稀释前的浓度相同 a、b、c三点溶液的pH由大到小顺序为a>b>c a点的Kw值比b点的Kw值大 a点水电离的c(H+)大于c点水电离的c(H+)
将NaOH溶液和氨水溶液各稀释一倍,二者的OH-浓度均减小到原来的一半 如果盐酸的浓度是醋酸浓度的两倍,则盐酸中的H+浓度是醋酸的两倍 强电解质溶液的导电能力一定比弱电解质溶液强 中和等体积、等物质的量浓度的盐酸和醋酸溶液,盐酸所需NaOH和醋酸所需NaOH相等
25℃,pH均为2的盐酸和CH3COOH溶液中溶质的物质的量浓度 将pH=4的盐酸和醋酸分别稀释成pH=5的溶液,所加水的量 同温、同浓度的NaCl溶液和氨水的导电能力 25℃时,pH均为3的HCl和FeCl3溶液中水的电离程度
某醋酸溶液的pH=a,将此溶液稀释10倍后,溶液的pH=a+1 在滴有酚酞的氨水里,加入NH4Cl至溶液恰好无色,则此时溶液的pH<7 常温下,1.0×10- 3 mol/L盐酸的pH=3.0,1.0×10- 8 mol/L 盐酸的pH=8.0 电解质不一定导电,导电物质不一定是电解质
强电解质溶液的导电能力一定比弱电解质溶液强 中和等体积、等物质的量浓度的盐酸和醋酸溶液,两者所需氢氧化钠一样多 如果盐酸的浓度是醋酸浓度的二倍,则盐酸的H+浓度也是醋酸的二倍 将NaOH和氨水溶液各稀释一倍,两者的OH-浓度均减少到原来的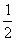
将NaOH和氨水各稀释一倍,两者的OH-浓度均减少到原来的二分之一 中和等体积、等物质的量浓度的盐酸和醋酸溶液,盐酸所需氢氧化钠等于醋酸 如果盐酸的浓度是醋酸浓度的二倍,则盐酸的H+浓度也是醋酸的二倍 强电解质溶液的导电能力一定比弱电解质溶液强
中和等体积,等pH的盐酸和醋酸溶液,盐酸所需氧氧化钠小于醋酸 强电解质溶液的导电能力一定比弱电质溶液强 将NaOH和氨水溶液各稀释一倍,两者的OH-浓度均减小到原来的一半 如果盐酸的浓度是醋酸溶液的二倍,则盐酸的H+浓度也是醋酸H+浓度的二倍
某醋酸溶液的pH=a,将此溶液稀释10倍后,溶液的pH=a+1 在滴有酚酞的氨水里,加入NH4Cl至溶液恰好无色,则此时溶液的pH<7 常温下,1.0×10- 3 mol/L盐酸的pH=3.0,1.0×10- 8 mol/L 盐酸的pH=8.0 电解质不一定导电,导电物质不一定是电解质
b、c两点溶液的导电能力不相同 a、b、c三点溶液中水的电离程度a>c>b c点溶液中C.(H+) + C(CH3COOH)= C(OH-) 用相同浓度的盐酸分别与等体积的b、c处溶液 反应,消耗盐酸体积Vb=Vc
相同pH的醋酸溶液和盐酸分别与同样颗粒大小的锌反应时,产生H2的起始速率相等 常温下,测得0.1 mol·L-1醋酸溶液的pH=4 常温下,将pH=1的醋酸溶液稀释1 000倍,测得pH<4 在相同条件下,醋酸溶液的导电性比盐酸的弱
强电解质溶液的导电能力一定比弱电解质溶液强 中和等体积、等物质的量浓度的盐酸和醋酸溶液,盐酸所需氢氧化钠等于醋酸 将氢氧化钠和氨水溶液各稀释一倍,两者的 OH-浓度均减少到原来的 1/2 如果盐酸的浓度是醋酸浓度的2倍,则盐酸的H+浓度也是醋酸的2倍
NaOH溶液的导电能力一定比氨水强 中和等体积、等物质的量浓度的盐酸和醋酸,需要等量的NaOH 若盐酸的浓度是醋酸浓度的两倍,则盐酸的c(H+)也是醋酸c(H+)的两倍 将NaOH溶液和氨水各稀释一倍,两者的c(OH-)均减小到原来的一半
弱电解质溶液的导电能力一定比强电解质溶液弱 将等体积、等浓度的NaOH溶液和氨水各稀释一倍后,两者中和等浓度盐酸的能力氨水强于NaOH溶液 物质的量浓度相同的磷酸钠溶液和磷酸溶液所含PO3-4浓度也相同 如果盐酸中c(H+)是醋酸溶液中c(H+)的2倍,则c (HCl) <2c (CH3COOH)
曲线Ⅱ为醋酸稀释时的变化曲线 a、b、c三点溶液的pH大小顺序为a>b>c a点的Kw值比b点的Kw值大 b点水电离的H+物质的量浓度小于c点水电离的H+物质的量浓度 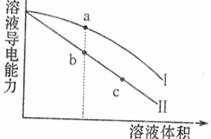
c(H+)>c(OH-)的溶液一定显酸性 将0.1 mol·L-1HI溶液加水稀释l00倍,溶液中所有离子的浓度随之减小 常温下pH=5的硫酸溶液稀释到原来的1000倍,稀释后c(SO42-)与c(H+)之比约为1∶20 常温下的纯水加热到40℃,pH减小
两溶液稀释前的浓度相同 a、b、c三点溶液的pH由大到小顺序为a>b>c a点的KW值比b点的KW值大 a点水电离的c(H+)大于c点水电离的c(H+)
溶液中导电粒子的数目增多,导电能力增强 醋酸的电离程度增大,c(H+)也增大 溶液中K.= 不变 醋酸的电离常数K.随醋酸浓度减小而减小
不变 醋酸的电离常数K.随醋酸浓度减小而减小
氨水溶液会使紫色石蕊溶液变红 常温下PH等于13的氨水溶液与PH等于1的盐酸溶液等体积混合后溶液的PH>7 常温下10ml的0.01mol/L氨水溶液测得PH值约为10 相同温度下,氨水导电能力比相同浓度氢氧化钠溶液的导电能力弱

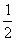

 不变 醋酸的电离常数K.随醋酸浓度减小而减小
不变 醋酸的电离常数K.随醋酸浓度减小而减小