
 A. 若保持入射点A.位置不变,将入射光线顺时针旋转,则从水面上方观察,b光先消失 在水中,b光波长比a光波长大 a、b两束光相比较,在真空中的传播速度a光比b光大 用同一双缝干涉实验装置做实验,a光的干涉条纹间距 大于b光的条纹间距
A. 若保持入射点A.位置不变,将入射光线顺时针旋转,则从水面上方观察,b光先消失 在水中,b光波长比a光波长大 a、b两束光相比较,在真空中的传播速度a光比b光大 用同一双缝干涉实验装置做实验,a光的干涉条纹间距 大于b光的条纹间距



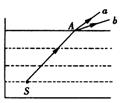

 A. a、b两束光相比较,a光的折射率较大 a、b两束光相比较,a光在水中的传播速度较大 若保持入射点A.位置不变,将入射光线顺时针旋转,则从水面上方观察,b光先消失 采用同一双缝干涉实验装置,分别以a、b光做光源,a光的干涉条纹间距小于b光的干涉条纹间距
A. a、b两束光相比较,a光的折射率较大 a、b两束光相比较,a光在水中的传播速度较大 若保持入射点A.位置不变,将入射光线顺时针旋转,则从水面上方观察,b光先消失 采用同一双缝干涉实验装置,分别以a、b光做光源,a光的干涉条纹间距小于b光的干涉条纹间距



 A.若保持入射点A.位置不变,将入射光线顺时针旋转,则从水面上方观察,b光先消失 用同一双缝干涉实验装置做实验,a光的干涉条纹间距大于b光的条纹间距 a、b两束光相比较,在真空中的传播速度a光比b光大 在水中,b光波长比a光波长大
A.若保持入射点A.位置不变,将入射光线顺时针旋转,则从水面上方观察,b光先消失 用同一双缝干涉实验装置做实验,a光的干涉条纹间距大于b光的条纹间距 a、b两束光相比较,在真空中的传播速度a光比b光大 在水中,b光波长比a光波长大