你可能感兴趣的试题
两种溶液的pH:盐酸大于醋酸
用相同浓度的NaOH溶液分别与等体积的盐酸和醋酸溶液恰好反应完全,盐酸消耗的NaOH溶液体积多
向醋酸中加入等物质的量的NaOH,溶液呈碱性,且溶液中
两种溶液中水电离出的氢离子:盐酸大于醋酸
溶液中pH醋酸比盐酸大 与足量的锌粉反应产生的氢气体积相同 与足量锌粒反应时,一开始盐酸的速率快 能中和NaOH溶液的物质的量醋酸较少
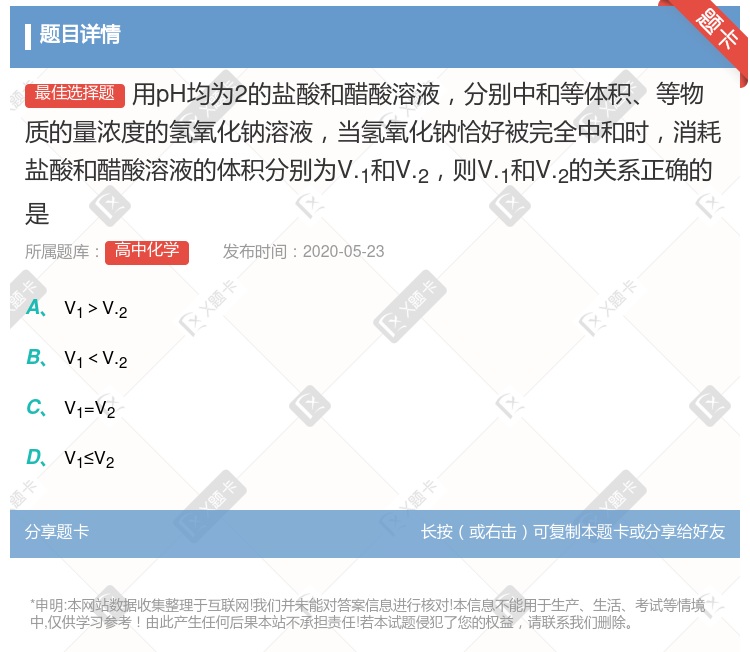
V.1>V.2 V.12 V.1=V.2 V.1≤V.2
两溶液物质的量浓度相同 用同浓度的盐酸中和时,消耗盐酸的体积相同 两溶液中OH-离子浓度相同 加入等体积的水稀释后,pH仍相等
醋酸和盐酸的浓度:c(CH3COOH)>c(HCl)
消耗盐酸和醋酸的体积:V12
醋酸与氢氧化钠溶液反应所得溶液:[Na+]>[CH3COO-]>[OH-]>[H+]
所得的两种溶液中:[Na+]相同;[CH3COO-]=[Cl-]
对含等物质的量浓度的醋酸和盐酸溶液分别做导电性实验,醋酸溶液灯泡相对较暗 等体积,等物质的量浓度的醋酸和盐酸,与同浓度同体积小苏打溶液反应,开始时放出气体的速率盐酸快,醋酸慢 中和等体积,等物质的量浓度的醋酸和盐酸,消耗同种氢氧化钠溶液的体积相同 1L浓度为0.1mol·L-1的CH3COOH溶液中,测得H+的物质的量约为0.003mol
用pH试纸测定并比较浓度均为0.1 mol/L的盐酸和醋酸的pH 用0.1 mol/L NaOH溶液分别中和等体积等浓度的盐酸和醋酸,比较消耗NaOH溶液的体积 各取1mL盐酸和醋酸溶液,分别测其pH,pH均为1,加水都稀释到1000倍,比较稀释后溶液的pH 用pH试纸测定并比较等浓度的氯化钠和醋酸钠两溶液的pH
两种溶液中,由水电离出的氢离子浓度均为l×10-11 mol·L-1
分别加水稀释100倍后,两种溶液的pH仍相等
中和同体积的这两种酸溶液所需要NaOH物质的量也相等
分别加入足量锌片,两种溶液生成H2的体积相等
强电解质溶液的导电能力一定比弱电解质溶液的导电能力强 因为CH3COOH是弱电解质,HCl是强电解质,所以中和等体积等物质的量浓度的醋酸和盐酸时,中和醋酸消耗的NaOH比盐酸消耗的NaOH用量少 物质的量浓度相同的磷酸钠溶液和磷酸溶液中PO43-的物质的量浓度相同 足量Zn分别和等体积、等物质的量浓度的盐酸和醋酸反应时,产生H2的量相同,放出H2的速率不等
两种溶液中,由水电离出的氢离子浓度均为l×10-11 mol·L-1
分别加水稀释100倍后,两种溶液的pH仍相等 中和同体积的这两种酸溶液所需要NaOH物质的量相等
分别加入足量锌片,两种溶液生成H2的体积相等
pH由小到大的顺序是①< ②< ③< ④ 溶液中水电离出的H+浓度由小到大的顺序是②<①<④<③ 取一定体积的④溶液,分别和①、②、③溶液完全中和,消耗①、②、③溶液的体积由小到大的顺序是②<①<③ 取a体积的①溶液和b体积的④溶液混合后,溶液的pH为3,则a:b约为11:9
稀释pH= 10的氨水,溶液中所有离子的浓度均降低 pH均为5的盐酸和氯化铵溶液中,水的电离程度相同 等浓度的碳酸钠与碳酸氢钠溶液相比,碳酸钠溶液的pH大 分别中和pH与体积均相同的硫酸和醋酸,硫酸消耗氢氧化钠的物质的量多
硫酸溶液的酸性一定比醋酸溶液的强 中和等体积、等pH的氨水和氢氧化钠溶液,需要盐酸的物质的量相同。 将等体积pH=2的盐酸和醋酸溶液均稀释到pH=3,加水的体积盐酸小于醋酸 84消毒液和洁厕剂均为酸性,可以混合使用
对含等物质的量浓度的醋酸和盐酸溶液分别做导电性实验,醋酸溶液灯泡相对较暗 等体积,等物质的量浓度的醋酸和盐酸,与同浓度同体积小苏打溶液反应,开始时放出气体的速率盐酸快,醋酸慢 1L浓度为0.1mol·L-1的CH3COOH溶液中,测得H+的物质的量约为0.003mol 中和等体积,等物质的量浓度的醋酸和盐酸,消耗同种氢氧化钠溶液的体积相同
中和等体积等浓度的醋酸和盐酸,醋酸需要的氢氧化钠溶液更多 pH=3的醋酸溶液,稀释至10倍后pH=4 pH=3的醋酸溶液与pH=11的氢氧化钠溶液等体积混合后pH>7 pH均为3的醋酸和盐酸分别与足量Zn反应,醋酸产生的H2多
稀释pH=10的氨水,溶液中所有离子的浓度均降低 pH均为5的盐酸和氯化铵溶液中,水的电离程度相同 等浓度的碳酸钠与碳酸氢钠溶液相比,碳酸钠溶液的pH大 分别中和pH与体积均相同的硫酸和醋酸,硫酸消耗氢氧化钠的物质的量多