你可能感兴趣的试题
锌电极是番茄电池的正极 番茄电池可将化学能转化为电能 番茄电池形成通路后,电子将从铜电极流出 将电压表直接接在该番茄电池上,会损坏电压表
锌电极是番茄电池的正极 番茄电池可将化学能转化为电能 番茄电池形成通路后,电子将从铜电极流出 将电压表直接接在该番茄电池上,会损坏电压表
锌片是负极 两个铜片上都发生氧化反应 石墨是阴极 两个番茄都形成原电池
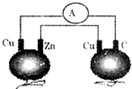 石墨是阴极 两个铜片上都发生氧化反应 两个番茄都形成原电池 锌片是负极
石墨是阴极 两个铜片上都发生氧化反应 两个番茄都形成原电池 锌片是负极
锌电极是番茄电池的正极 番茄电池可将化学能转化为电能 番茄电池形成通路后,电子将从铜电极流出 将电压表直接接在该番茄电池上,会损坏电压表
锌电极是番茄电池的正极
番茄电池可将化学能转化为电能
电压表读数为4V
将电压表直接接在该番茄电池上,会损坏电压表
锌片是负极 两个铜片上都发生氧化反应 石墨是阴极 两个番茄都形成原电池
一段时间后,锌片质量会变小 铜片上发生氧化反应 电子由铜片通过导线流向锌 锌电极是该电池的正极
锌片是负极 两个铜片上都发生氧化反应 石墨是阴极 两个番茄都形成原电池
。这里的“13μA.”是指 A.电路中的电流 电路中的总电阻 水果电池的电动势 铜片与锌片间的电压 
实验①、②说明锌能与稀硫酸反应而铜不能 实验③说明发生原电池反应时会加快化学反应速率 实验③说明在该条件下铜可以与稀硫酸反应生成氢气 实验④说明该原电池中铜为正极、锌为负极
两个铜片上都发生还原反应 锌片是阴极 石墨电极上发生还原反应 两个番茄都形成原电池
锌电极是番茄电池的正极
番茄电池可将化学能转化为电能
番茄电池形成通路后,电子将从铜电极流出
将电压表直接接在该番茄电池上,会损坏电压表
锌电极是番茄电池的正极 番茄电池可将化学能转化为电能 番茄电池形成通路后,电子将从铜电极流出 将电压表直接接在该番茄电池上,会损坏电压表
锌电极是番茄电池的正极 番茄电池可将化学能转化为电能 番茄电池形成通路后,电子将从铜电极流出 将电压表直接接在该番茄电池上,会损坏电压表
锌片是负极 两个铜片上都发生氧化反应 石墨是阴极 两个番茄都形成原电池
锌电极是番茄电池的正极
番茄电池可将化学能转化为电能
番茄电池形成通路后,电子将从铜电极流出
将电压表直接接在该番茄电池上,会损坏电压表
锌片是负极 两个铜片上都发生氧化反应 石墨是阴极 两个番茄都形成原电池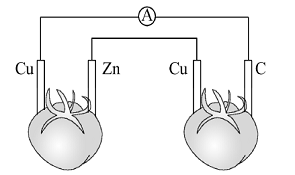
锌电极是番茄电池的正极 番茄电池可将化学能转化为电能 番茄电池形成通路后,电子将从铜电极流出 将电压表直接接在该番茄电池上,会损坏电压表
一段时间后,锌片质量会变小 铜片上发生氧化反应 电子由铜片通过导线流向锌片 锌电极是该电池的正极

 石墨是阴极 两个铜片上都发生氧化反应 两个番茄都形成原电池 锌片是负极
石墨是阴极 两个铜片上都发生氧化反应 两个番茄都形成原电池 锌片是负极

