
 +5C2O
+5C2O +16H+ ==2Mn2+ +10CO2↑+8H2O 在NH4HSO4溶液中缓慢滴入含等物质的量的NaOH的溶液:NH
+16H+ ==2Mn2+ +10CO2↑+8H2O 在NH4HSO4溶液中缓慢滴入含等物质的量的NaOH的溶液:NH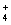 +OH—==NH3·H2O VO2+与酸性高锰钾溶液反应:5VO2++MnO
+OH—==NH3·H2O VO2+与酸性高锰钾溶液反应:5VO2++MnO +H2O==5VO
+H2O==5VO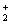 +Mn2++2H+ Fe2+ 被空气氧化:4Fe2+ +O2+2H2O == 4Fe3+ +4OH—
+Mn2++2H+ Fe2+ 被空气氧化:4Fe2+ +O2+2H2O == 4Fe3+ +4OH—
 2OH-- + H2↑ + Cl2↑
2OH-- + H2↑ + Cl2↑
 4OH-
4OH-
 ,Mn2+,H+ Pt(+) (-)Fe Fe3+,Fe2+ Mn
,Mn2+,H+ Pt(+) (-)Fe Fe3+,Fe2+ Mn ,Mn2+,H+ Mn(+) (-)Pt Mn
,Mn2+,H+ Mn(+) (-)Pt Mn ,Mn2+,H+ Fe3+,Fe2+ Pt(+) (-)Pt Fe2+,Fe3+
,Mn2+,H+ Fe3+,Fe2+ Pt(+) (-)Pt Fe2+,Fe3+
 +5C2O
+5C2O +16H+===2Mn2++10CO2↑+8H2O 在NH4HSO4溶液中缓慢滴入含等物质的量的NaOH的溶液:NH
+16H+===2Mn2++10CO2↑+8H2O 在NH4HSO4溶液中缓慢滴入含等物质的量的NaOH的溶液:NH +OH-===NH3·H2O VO2+与酸性高锰酸钾溶液反应: 5VO2++MnO
+OH-===NH3·H2O VO2+与酸性高锰酸钾溶液反应: 5VO2++MnO +H2O===5VO
+H2O===5VO +Mn2++2H+ FeI2溶液中滴入过量溴水:2Fe2++2I-+2Br2===2Fe3++I2+4Br-
+Mn2++2H+ FeI2溶液中滴入过量溴水:2Fe2++2I-+2Br2===2Fe3++I2+4Br-