你可能感兴趣的试题
a和b不连接时,铁片上会有金属铜析出 a和b用导线连接时,铜片上发生的反应为:Cu2++2e﹣=Cu 无论a和b是否连接,铁片均会溶解,溶液从蓝色逐渐变成浅绿色 a和b分别连接直流电源正、负极,电压足够大时,Cu2+向铜电极移动
安全气囊传感器紧固件的拧紧力矩不正确,会导致气囊不正确的张开 在维修安全气囊中的部件之前拆掉蓄电池搭铁电缆 在处理充气之后的气囊时戴安全护镜和防护手套 用自备电源的万用表以确定系统工作状态是否正常
电化学腐蚀原理是电池作用原理 有电位不同的两个极 两极在同一电解质溶液中 在阴极发生氧化反应,在阳极发生还原反应
a电极为该电池负极 O2在b电极上得电子,被氧化 电池工作时,a电极反应式: CH3OCH3-12e-+3H2O===2CO2↑+12H+ 电池工作时,燃料电池内部H.+从a电极移向b电极
锌是负极,电子从锌片经导线流向铜片 氢离子在铜片表面被还原 锌质量减少65g时,铜电极表面析出氢气是22.4L 装置中存在“化学能→电能→光能”的转换
多孔金属a是负极 O2在b电极上发生还原反应 a电极上的电极反应式:H2-2eˉ==2H+ 放电前后电解质溶液的pH 发生改变
该净水器工作时没有化学变化 该净水装置中活性炭的作用是吸附 该净水器的净水原理是过滤、吸附和蒸馏 该净水器除去水中部分杂质,净化后的水属于混合物
锌是负极,电子从锌片经导线流向铜片 铜片表面有气泡生成 如果将硫酸换成橙汁,导线中不会有电子流动 装置中存在“化学能→电能→光能”的转换
a极为负极 b极的电极反应式为O2+4e-+2H2O=4OH- 电子流向:a经外电路流向b 该传感器工作一段时间后,电解质溶液的pH值将变大
铁管道与直流电源负极相连,防止铁管道腐蚀 小苏打、氢氧化铝可用于治疗胃酸过多
分子由原子构成 该反应属于置换反应 原子在化学反应中不可再分 化学反应前后原子的种类和数目不变 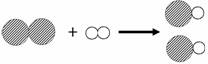
科学管理原理是由泰勒提出的 现代工效学的基本指导思想是以人为本 人际关系理论认为工作是“经济人”而不是“社会人” 工作特征模型包含五个核心维度
电池工作时,电子的流向:锂电极→导线→碳电极 水既是氧化剂又是溶剂,有机电解质可用水溶液代替 电池总反应为2Li+2H2O=2LiOH+H2↑ 该装置不仅可提供电能,还可得到清洁燃料氢气
电源的电动势为6.0V. 电源的内阻为2 Ω 电源的短路电流为0.5A. 当外电阻为2 Ω时电源的输出功率最大 
电表中的铝框就是为了绕线圈方便 扼流圈的作用原理就是利用自感效应 电磁炉的工作原理就是利用涡流热效应 变压器的铁芯做成薄片叠合就是为了减少涡流损耗
放电过程中,负极质量会增加 Ag2O 电极发生还原反应 Zn 电极的电极反应式:Zn-2eˉ+2OHˉ=Zn(OH)2 放电前后电解质溶液的碱性保持不变
锌是负极,电子从锌片经导线流向铜片 铜片表面有气泡生成 如果将硫酸换成橙汁,导线中不会有电子流动 装置中存在“化学能→电能→光能”的转换
Zn电极是负极 Ag2O电极上发生还原反应 Zn电极的电极反应式:Zn﹣2e﹣+2OH﹣═Zn(OH)2 放电前后电解质溶液的pH保持不变
科学管理原理是由泰勒提出的 现代工效学的基本指导思想是以人为本 人际关系理论认为工作是“经济人”而不是“社会人” 工作特征模型包含五个核心维度
该反应为置换反应 反应物都是化合物 原子是化学变化中的最小粒子 化学反应前后,原子的种类和数目不变