你可能感兴趣的试题
Br―2+― I.―2+― Br――2+ Fe2+――
I.->Fe2+>Cl->SO2 Cl->Fe2+>SO2>I.- Fe2+>I.->Cl->SO2 SO2>I.->Fe2+>Cl-
该溶液中,K+、Fe2+、C6H5OH、Br-可以大量共存 和KI溶液反应的离子方程式:Fe3++2I-===Fe2++I2 和Ba(OH)2溶液反应的离子方程式:Fe3++SO +Ba2++3OH-===Fe(OH)3↓+ BaSO4↓ 1 L 0.1 mol·L-1该溶液和足量的Zn充分反应,生成11.2 g Fe
+Ba2++3OH-===Fe(OH)3↓+ BaSO4↓ 1 L 0.1 mol·L-1该溶液和足量的Zn充分反应,生成11.2 g Fe
该溶液中,K+、Fe2+、C6H5OH、Br-可以大量共存 和KI溶液反应的离子方程式:Fe3++2I-===Fe2++I2 和Ba(OH)2溶液反应的离子方程式:Fe3++SO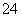 +Ba2++3OH-===Fe(OH)3↓+ BaSO4↓ 1 L 0.1 mol·L-1该溶液和足量的Zn充分反应,生成11.2 g Fe
+Ba2++3OH-===Fe(OH)3↓+ BaSO4↓ 1 L 0.1 mol·L-1该溶液和足量的Zn充分反应,生成11.2 g Fe
该溶液中,K+、Fe2+、C6H5OH、Br-可以大量共存 和KI溶液反应的离子方程式:Fe3++2I-==Fe2++I2 和Ba(OH)2溶液反应的离子方程式: Fe3++SO42-+Ba2++3OH-==Fe(OH)3↓+BaSO4↓ 1L0.1mol·L-1该溶液和足量的Zn充分反应,生成11.2gFe
该溶液中,K+、Fe2+、C6H5OH、Br-可以大量共存 和KI溶液反应的离子方程式:Fe3++2I-=Fe2++I2 和Ba(OH)2溶液反应的离子方程式:Fe3++SO42-+Ba2++3OH-=Fe(OH)3↓+BaSO4↓ 1 L 0.1 mol·L-1该溶液和足量的Zn充分反应,生成11.2 g Fe
该溶液中,H+、Mg2+、NO3-、Cl-可以大量共存 该溶液能使淀粉碘化钾试纸变蓝,反应的离子方程式为:Fe3++ 2I-= Fe2++ I2 该溶液和足量Ba(OH)2溶液反应的离子方程式为: Fe3++ SO42-+ Ba2++3OH-=Fe(OH)3↓+BaSO4↓ 该溶液与足量铜粉反应的离子方程式为:3Cu+2Fe3+=2Fe+3Cu2+
该溶液中,K+、Fe2+、C6H5OH、Br- 可以大量共存 和KI溶液反应的离子方程式:Fe3++2I -= Fe2++I2 和Ba(OH)2溶液反应的离子方程式:Fe3++SO42-+Ba2++3OH-=Fe(OH)3↓+BaSO4↓ 1L 0.1mol·L-1该溶液和足量的Zn充分反应,生成11.2g Fe
单质铜与稀硝酸反应:Cu + 2 H+ + 2 NO3- ==Cu2+ + 2 NO↑+ H2O NaOH溶液与足量的Ca(HCO3)2溶液反应:2HCO3- + 2OH- + Ca2+==CaCO3↓+ 2H2O 等物质的量的FeBr2和Cl2在溶液中的反应:2Fe2+ + 2Br - + 2Cl2==2Fe3+ + Br2 + 4Cl - 氨水吸收少量的二氧化硫:2NH3·H2O + SO2==2NH4+ +SO32- + H2O
该溶液中,K+、Fe2+、C6H5OH、Br-可以大量共存
和KI溶液反应的离子方程式:Fe3+ + 2I-= Fe2+ + I2 和Ba(OH)2溶液反应的离子方程式:Fe3+ + SO42-+ Ba2+ + 3OH-= Fe(OH)3↓+ BaSO4↓
1L0.1mol/L该溶液和足量的Zn充分反应,生成 11.2gFe
Br-、Fe2+、I- I-、Fe2+、Br- Br-、I-、Fe2+ Fe2+、I-、Br-
碳酸钙溶于稀盐酸中:CO32-+2H+═H2O+CO2↑
氯化钡溶液与稀硫酸反应:Ba2++SO42-═BaSO4↓
铁与稀盐酸反应:2Fe+6H+═3H2↑+2Fe3+
铜片插入硝酸银溶液中:Cu+Ag+═Cu2++Ag
铁与氯化铁溶液反应:Fe+Fe3+=2Fe2+ 大理石与稀盐酸反应:CO32﹣+2H+=CO2↑+H2O 铜与稀硫酸反应:Cu+2H+=Cu2++H2↑ 氯气与氢氧化钠溶液反应:Cl2+2OH﹣=Cl﹣+ClO﹣+H2O
实验①和③中的铁钉只作还原剂 上述实验证明氧化性:Fe3+>Fe2+>Cu2+ 实验②中Fe2+既显氧化性又显还原性 实验③中反应的离子方程式为Fe+Fe3+===2Fe2+

 +Ba2++3OH-===Fe(OH)3↓+ BaSO4↓ 1 L 0.1 mol·L-1该溶液和足量的Zn充分反应,生成11.2 g Fe
+Ba2++3OH-===Fe(OH)3↓+ BaSO4↓ 1 L 0.1 mol·L-1该溶液和足量的Zn充分反应,生成11.2 g Fe
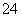 +Ba2++3OH-===Fe(OH)3↓+ BaSO4↓ 1 L 0.1 mol·L-1该溶液和足量的Zn充分反应,生成11.2 g Fe
+Ba2++3OH-===Fe(OH)3↓+ BaSO4↓ 1 L 0.1 mol·L-1该溶液和足量的Zn充分反应,生成11.2 g Fe