你可能感兴趣的试题
同时改变两个变量来研究反应速率的变化,能更快得出有关规律 对于同一个化学反应,无论是一步完成还是分几步完成,其反应的焓变相同 已知2C(s)+2O2(g)=2CO2(g) △H1;2C(s)+O2(g)=2CO(g) △H2,则△H1>△H2 一定条件下,使用催化剂能加快反应速率并提高反应物的平衡转化率
和2 mol 放入2L.密闭容器中发生反应2A(g) + B(g) 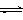 2C(g) ΔH.<0。4 s后反应达到平衡状态,此时测得 的浓度为0.6 mol/L。下列说法正确的是A.4 s内,υB.=0.075 mol/(L ·s)B.当c(A.)︰c(B.)︰c(C.)=2︰1︰2 时,该反应即达到平衡状态C.达到平衡状态后,若只升高温度,则C.的物质的量浓度增大 达到平衡状态后,若温度不变,缩小容器的体积,则A.的转化率降低
2C(g) ΔH.<0。4 s后反应达到平衡状态,此时测得 的浓度为0.6 mol/L。下列说法正确的是A.4 s内,υB.=0.075 mol/(L ·s)B.当c(A.)︰c(B.)︰c(C.)=2︰1︰2 时,该反应即达到平衡状态C.达到平衡状态后,若只升高温度,则C.的物质的量浓度增大 达到平衡状态后,若温度不变,缩小容器的体积,则A.的转化率降低
对于反应nA(g)+B (g) 2C(g),平衡后增大压强,A.的百分含量减小,则n≥2。 对于反应2A(g)
2C(g),平衡后增大压强,A.的百分含量减小,则n≥2。 对于反应2A(g) B(g)△H.<0,恒温恒容,压强不再变化说明反应达到平衡状态。 对于反应2A(g)
B(g)△H.<0,恒温恒容,压强不再变化说明反应达到平衡状态。 对于反应2A(g) B(g),恒温恒容条件下,气体密度不变,说明达到平衡状态 对于反应2A(g)
B(g),恒温恒容条件下,气体密度不变,说明达到平衡状态 对于反应2A(g) B(g),若v(A.)正=2v(B.)逆,说明反应达到平衡状态
B(g),若v(A.)正=2v(B.)逆,说明反应达到平衡状态
2A(l)+B(l)=2C(g) △H1 2A(g)+B(g)=2C(g) △H2 2A(g)+B(g)=2C(l) △H3 2A(l)+B(l)=2C(l) △H4
对于反应nA(g)+B (g) 2C(g),平衡后增大压强,A.的百分含量减小,则n≥2。 对于反应2A(g)
2C(g),平衡后增大压强,A.的百分含量减小,则n≥2。 对于反应2A(g) B.(g) △H.<0,若体系温度不再变化说明反应达到平衡状态。 对于反应2A(g)
B.(g) △H.<0,若体系温度不再变化说明反应达到平衡状态。 对于反应2A(g) B.(g),恒温,恒容条件下气体密度不再变化,说明反应达到平衡状态 对于反应2A(g)
B.(g),恒温,恒容条件下气体密度不再变化,说明反应达到平衡状态 对于反应2A(g) B.(g),若vA.正=2vB.逆,说明反应达到平衡状态
B.(g),若vA.正=2vB.逆,说明反应达到平衡状态
2A(l)+ (l)===2C(g) ΔH.1 B. 2A(g)+B.(g)===2C(l) ΔH.2 2A(g)+B.(g)===2C(g) ΔH.3 2A(l)+B.(l)===2C(l) ΔH.4
A.C.均为固体 A是气体, 是固体 C.A.C.均为气体 A为固体,C.为气体
和2 mol 放入2L.密闭容器中发生反应2A(g) + B(g) 2C(g) ΔH.<0。4 s后反应达到平衡状态,此时测得 的浓度为0.6 mol/L。下列说法正确的是( ) A.4 s内,υB.=0.075 mol/(L ·s) B.当cA.︰cB.︰cC.=2︰1︰2 时,该反应即达到平衡状态 C.达到平衡状态后,若只升高温度,则C.的物质的量浓度增大 达到平衡状态后,若温度不变,缩小容器的体积,则A.的转化率降低
2C(g) ΔH.<0。4 s后反应达到平衡状态,此时测得 的浓度为0.6 mol/L。下列说法正确的是( ) A.4 s内,υB.=0.075 mol/(L ·s) B.当cA.︰cB.︰cC.=2︰1︰2 时,该反应即达到平衡状态 C.达到平衡状态后,若只升高温度,则C.的物质的量浓度增大 达到平衡状态后,若温度不变,缩小容器的体积,则A.的转化率降低
和足量 ,发生反应如下:2A(g)+B.(s)2C(g),测得相关数据如下,分析可知下列说法不正确的是 A.实验Ⅲ的化学平衡常数K.<1B.实验放出的热量关系为b=2a 实验Ⅲ在30 min达到平衡,30 min内A.的速率:vA.=0.002 5 mol·L.-1·min-1 当容器内气体密度不随时间而变化时上述反应达到平衡
放热反应 吸热反应 没有显著的热量变化 原化学平衡没有发生移动

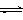 2C(g) ΔH.<0。4 s后反应达到平衡状态,此时测得 的浓度为0.6 mol/L。下列说法正确的是A.4 s内,υB.=0.075 mol/(L ·s)B.当c(A.)︰c(B.)︰c(C.)=2︰1︰2 时,该反应即达到平衡状态C.达到平衡状态后,若只升高温度,则C.的物质的量浓度增大 达到平衡状态后,若温度不变,缩小容器的体积,则A.的转化率降低
2C(g) ΔH.<0。4 s后反应达到平衡状态,此时测得 的浓度为0.6 mol/L。下列说法正确的是A.4 s内,υB.=0.075 mol/(L ·s)B.当c(A.)︰c(B.)︰c(C.)=2︰1︰2 时,该反应即达到平衡状态C.达到平衡状态后,若只升高温度,则C.的物质的量浓度增大 达到平衡状态后,若温度不变,缩小容器的体积,则A.的转化率降低
 2C(g),平衡后增大压强,A.的百分含量减小,则n≥2。 对于反应2A(g)
2C(g),平衡后增大压强,A.的百分含量减小,则n≥2。 对于反应2A(g) B(g)△H.<0,恒温恒容,压强不再变化说明反应达到平衡状态。 对于反应2A(g)
B(g)△H.<0,恒温恒容,压强不再变化说明反应达到平衡状态。 对于反应2A(g) B(g),恒温恒容条件下,气体密度不变,说明达到平衡状态 对于反应2A(g)
B(g),恒温恒容条件下,气体密度不变,说明达到平衡状态 对于反应2A(g) B(g),若v(A.)正=2v(B.)逆,说明反应达到平衡状态
B(g),若v(A.)正=2v(B.)逆,说明反应达到平衡状态
 2C(g),平衡后增大压强,A.的百分含量减小,则n≥2。 对于反应2A(g)
2C(g),平衡后增大压强,A.的百分含量减小,则n≥2。 对于反应2A(g) B.(g) △H.<0,若体系温度不再变化说明反应达到平衡状态。 对于反应2A(g)
B.(g) △H.<0,若体系温度不再变化说明反应达到平衡状态。 对于反应2A(g) B.(g),恒温,恒容条件下气体密度不再变化,说明反应达到平衡状态 对于反应2A(g)
B.(g),恒温,恒容条件下气体密度不再变化,说明反应达到平衡状态 对于反应2A(g) B.(g),若vA.正=2vB.逆,说明反应达到平衡状态
B.(g),若vA.正=2vB.逆,说明反应达到平衡状态
 2C(g) ΔH.<0。4 s后反应达到平衡状态,此时测得 的浓度为0.6 mol/L。下列说法正确的是( ) A.4 s内,υB.=0.075 mol/(L ·s) B.当cA.︰cB.︰cC.=2︰1︰2 时,该反应即达到平衡状态 C.达到平衡状态后,若只升高温度,则C.的物质的量浓度增大 达到平衡状态后,若温度不变,缩小容器的体积,则A.的转化率降低
2C(g) ΔH.<0。4 s后反应达到平衡状态,此时测得 的浓度为0.6 mol/L。下列说法正确的是( ) A.4 s内,υB.=0.075 mol/(L ·s) B.当cA.︰cB.︰cC.=2︰1︰2 时,该反应即达到平衡状态 C.达到平衡状态后,若只升高温度,则C.的物质的量浓度增大 达到平衡状态后,若温度不变,缩小容器的体积,则A.的转化率降低