你可能感兴趣的试题
NH4NO3是一种常见的氮肥 NH4NO3中含2种不同的原子团 N
该反应中NH3被还原 该反应中H.-是还原剂 该反应中NH2-是还原产物 反应中被氧化和被还原的元素都是H.元素
NH4NO3中N.元素化合价依次为-1、+1价 该样品可能是纯净物 该样品硝酸铵的质量分数为70.0% 该样品可能混入了碳酸氢铵
NH4NO3 Ca(H2PO4)2 (NH4)2HPO4 KNO3
CO(NH2)2分子中氢氧元素的质量比为1:4 CO(NH2)2的一个分子有1个碳原子,1个氧原子2个氮原子和4个氢原子构成 CO(NH2)2中氮元素的质量分数计算式是14/60×100% CO(NH2)2由四种元素组成
氖气:Ne 氧化镁中镁元素显+2价: 氨气(NH3)中氮元素的化合价: 工业上炼铁原理:3C+2Fe2O3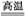 4Fe+3CO2↑
4Fe+3CO2↑
氮气经固氮后才能被植物吸收 氮元素在生物群落中以有机物形式传递 在缺氮时,土壤中的一些细菌可将硝酸盐最终转化为氮气 硝化细菌能把NH3氧化为植物生命活动需要的部分能量
甲、乙、丙三种物质中都含有氮元素 反应II、III和Ⅳ的氧化剂相同 VI的产物可在上述流程中被再次利用 V.中发生反应:NH3 + CO2 + H2O + NaCl === NaHCO3↓ + NH4Cl
氖气:Ne 氧化镁中镁元素显+2价: 氨气(NH3)中氮元素的化合价: 工业上炼铁原理:3C+2Fe2O3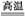 4Fe+3CO2↑
4Fe+3CO2↑
反应Ⅱ、III和Ⅳ的氧化剂一定相同 甲、乙、丙三种物质中都含有氮元素 反应Ⅵ的部分产物可在上述流程中循环利用 反应V.的化学方程式为NH3+CO2+H2O+NaCl==NaHCO3↓+NH4Cl
该反应属于分解反应 上述反应中氮元素的化合价发生了变化 施用碳铵时应注意用泥土掩埋 通过闻气味即可鉴别碳铵与氯化钾
NH4NO3是一种常见的氮肥 NH4NO3中含2种不同的原子团 N
的原料。工业上将金属钠于97~100℃熔融,向反应容器中缓慢通入无水液氨(NH3),再加热至一定温度生成氨基钠和氢气。下列说法不正确的是 A. NaNH2中氮元素的化合价为-3价 NaNH2中钠元素的质量分数为35.9% 钠的熔点比铁的熔点低 该反应的化学方程式为:4Na + 4NH3 △ 4NaNH2 + H2↑
①中N2与O2反应生成NO ②中合成氨属于人工固氮 ③中氮元素被氧化 氧元素参与了氮循环
NH4NO3是一种常见的氮肥 NH4NO3中含2种不同的原子团 N
原子的最外层均有5个电子,最高价均为+5价 非金属性比同周期的氧族元素和卤族元素弱 原子半径比同周期的氧族元素、卤族元素小 稳定性:NH3 > PH3
CO(NH2)2中氢、氧元素的质量比为1:4 CO(NH2)2的一个分子由1个碳原子、1个氧原子、2个氮原子和4个氢原子构成 CO(NH2)2中氮元素的质量分数计算式是嚣×100% CO(NH2)2由四种元素组成 )
元素的化合价是元素的原子在形成化合物时才表现出来的性质 在氢气中氢元素的化合价为+1 在水中氧元素的化合价为-2 在NH3中氮元素的化合价为-3
X.是N2O5 可用排水法收集NO、NO2气体 工业上以NH3、空气、水为原料生产硝酸 由NH3→N2,从原理上看,NH3可与NO2反应实现

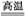 4Fe+3CO2↑
4Fe+3CO2↑
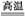 4Fe+3CO2↑
4Fe+3CO2↑