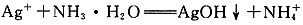你可能感兴趣的试题
KI氧化剂 KIO3还原剂 I2既是氧化产物又是还原产物 该反应是复分解反应
40 ℃之前与40 ℃之后溶液变蓝的时间随温度的变化趋势相反 图中b、c两点对应的NaHSO3反应速率相等 图中a点对应的NaHSO3反应速率为 5. 0×10-5 mol·L-1·s1- 温度高于40 ℃时,淀粉不宜用作该实验的指示剂
用铂丝蘸取少量某溶液进行焰色反应,火焰呈黄色,该溶液一定是钠盐溶液 将Fe(NO3)2样品溶于稀盐酸中,然后滴加KSCN溶液,溶液变红,说明Fe(NO3)2样品已氧化变质 在食盐试样中加入盐酸和KI溶液,加入淀粉溶液后变蓝,说明食盐试样中可能含有KIO3 加入AgNO3溶液后生成白色沉淀,加稀盐酸沉淀不溶解时,可确定有Cl-存在
KI氧化剂 KIO3还原剂 I2既是氧化产物又是还原产物 该反应是复分解反应
少量明矾溶液加入到过量NaOH溶液中 往FeCl3溶液中滴入KI溶液,再滴入淀粉溶液 少量Na2O2固体加入到过量NaHSO3溶液中 往酸性高锰酸钾溶液中滴入少量Fe2(SO4)3溶液
KIO3属于氧化物 KIO3中碘的化合价为+2 加碘食盐中的碘是指碘单质 加碘食盐可预防甲状腺肿大
少量明矾溶液加入到过量NaOH溶液中 往FeCl3溶液中滴入KI溶液,再滴入淀粉溶液 少量Na2O2固体加入到过量NaHSO3溶液中 往高锰酸钾酸性溶液中滴入少量Fe2(SO4)3稀溶液
少量明矾溶液加入到过量NaOH溶液中 往FeCl3溶液中滴入KI溶液,再滴入淀粉溶液 少量Na2O2固体加入到过量NaHSO4溶液中 往酸性高锰酸钾溶液中滴入少量Fe2(SO4)3稀溶液
40℃之前与40℃之后溶液变蓝的时间随温度的变化趋势相反 图中b、c两点对应的NaHSO3反应速率相等 图中a点对应的NaHSO3反应速率为5.0×10-5mol·L-1·s-1 温度高于40℃时,淀粉不宜用作该试验的指示剂
少量明矾溶液加入到过量NaOH溶液中 往FeCl3溶液中滴入KI溶液,再滴入淀粉溶液 少量Na2O2固体加入到过量NaHSO3溶液中 往酸性高锰酸钾溶液中滴入足量FeSO4浓溶液
少量明矾溶液加入到过量NaOH溶液中 往FeCl3溶液中滴入KI溶液,再滴入淀粉溶液 少量Na2O2固体加入到过量NaHCO3溶液中 在酸性高锰酸钾溶液中滴入少量Fe2(SO4)3稀溶液
0.1752 0.08760 0.2628 0.5840
在整个反应过程中,起催化作用的物质是KI 上述两个反应中,反应速率较快的是② 时钟反应的快慢由反应②决定 “溶液突然变为蓝色,随之又很快消失”这一现象与①②的反应速率有关
石灰乳与Na2CO3溶液混合: NH4HSO3溶液与足量NaOH溶液混合加热:
NH4HSO3溶液与足量NaOH溶液混合加热: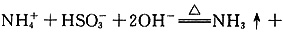
 酸性条件下KIO3溶液与KI溶液反应生成I2:
酸性条件下KIO3溶液与KI溶液反应生成I2: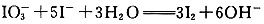 AgNO3溶液中加入过量氨水:
AgNO3溶液中加入过量氨水: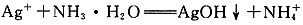

 NH4HSO3溶液与足量NaOH溶液混合加热:
NH4HSO3溶液与足量NaOH溶液混合加热: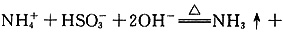
 酸性条件下KIO3溶液与KI溶液反应生成I2:
酸性条件下KIO3溶液与KI溶液反应生成I2: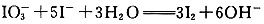 AgNO3溶液中加入过量氨水:
AgNO3溶液中加入过量氨水: