你可能感兴趣的试题
A.的转化率增大 平衡向逆反应方向移动 平衡没有移动 上述三种情况都有可能
第2 min时,如果只改变某一条件,则改变的条件可能是降低温度 第4 min至第6 min该化学反应处于平衡状态 第2 min时,如果只改变某一条件,则改变的条件可能是使用催化剂 第6 min时,其他条件不变,如果升高温度,正逆反应速率均增大
SiO2溶于水且显酸性 点燃是H2和Cl2化合的惟一条件 SiO2是酸性氧化物,它不溶于任何酸 液氯和氯水不是同一物质
化学平衡常数K.只与温度有关,随温度的升高,K.可能增大、减小或不变 催化剂不能改变平衡常数的大小 若某一条件的改变,使平衡常数发生了变化,则化学平衡必发生移动 化学平衡移动时,平衡常数不一定改变
第2 min时,如果只改变某一条件,则改变的条件可能是降低温度 第4 min至第6 min该化学反应处于平衡状态 第2 min时,如果只改变某一条件,则改变的条件可能是使用催化剂 第6 min时,其他条件不变,如果升高温度,正逆反应速率均增大
再通入少量氯气,c(H+)/ c(ClO-) 减小 通入少量SO2,溶液漂白性增强 加入少量固体NaOH,一定有c(Na+)=c(Cl-)+c(ClO-) 加入少量水,水的电离平衡向正反应方向移动
化学反应速率发生了改变 有气态物质参加的可逆反应达到平衡后,改变压强 由于某一条件的改变,使平衡混合物中各组分的浓度发生了不同程度的改变 可逆反应达到平衡后,使用催化剂
第2 min时,如果只改变某一条件,则改变的条件可能是降低温度 第4 min至第6 min该化学反应处于平衡状态 第2 min时,如果只改变某一条件,则改变的条件可能是使用催化剂 第6 min时,其他条件不变,如果升高温度,正逆反应速率均增大
再通入少量氯气,c(H+)/c(ClO-)减小
通入少量SO2,溶液漂白性增强
加入少量固体NaOH,一定有c(Na+)=c(Cl-)+c(ClO-)
加入少量水,水的电离平衡向正反应方向移动
第2 min时,如果只改变某一条件,则改变的条件可能是降低温度 第4 min至第6 min该化学反应处于平衡状态 第2 min时,如果只改变某一条件,则改变的条件可能是使用催化剂 第6 min时,其他条件不变,如果升高温度,正逆反应速率均增大
A.的转化率增大 平衡向逆反应方向移动 平衡没有移动 上述三种情况都有可能
再通入少量氯气,c(H+)/c( )减小 通入少量HCl,溶液漂白性增强 加入少量固体NaOH,一定有c(Na+)=c(
)减小 通入少量HCl,溶液漂白性增强 加入少量固体NaOH,一定有c(Na+)=c(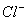 )+c(
)+c( ) 加入少量水,水的电离平衡向正反应方向移动
) 加入少量水,水的电离平衡向正反应方向移动
化学反应速率发生了改变 有气态物质参加的可逆反应达到平衡后,改变了压强 由于某一条件的改变,使平衡混合物中各组分的浓度发生了不同程度的改变 可逆反应达到平衡后,加入了催化剂
化学反应速率发生了改变 有气态物质参加的可逆反应达到平衡后,改变了压强 由于某一条件的改变,使平衡混合物中各组分的浓度发生了不同程度的改变 可逆反应达到平衡后,使用催化剂
化学反应速率发生了改变 有气态物质参加的可逆反应达到平衡后,改变了压强 由于某一条件的改变,使平衡混合物中各组分的浓度发生了不同程度的改变 可逆反应达到平衡后,使用催化剂
再通入少量氯气, 减小 通入少量SO2,溶液漂白性增强 加入少量固体NaOH,一定有c(Na+)=c(Cl-)+c(ClO-) 加入少量水,水的电或平衡向正反应方向移动
减小 通入少量SO2,溶液漂白性增强 加入少量固体NaOH,一定有c(Na+)=c(Cl-)+c(ClO-) 加入少量水,水的电或平衡向正反应方向移动
化学反应速率发生了改变 有气态物质参加的可逆反应达到平衡后,改变压强 由于某一条件的改变,使平衡混合物中各组分的浓度发生了不同程度的改变 可逆反应达到平衡后,使用催化剂
在该温度下,保持容积固定不变,向容器内补充了 气体,则a若其他条件不变,升高温度,则有a若保持温度、压强不变,充入惰性气体,则有a>b
(g)+n (g)  p (g)+q (g),在密闭容器中反应达到平衡,改变某一条件后,正反应速率增大,则下列说法正确的是( ) A.A.的转化率增大B.平衡向逆向移动 C.平衡没有移动D.上述三种情况都有可能
p (g)+q (g),在密闭容器中反应达到平衡,改变某一条件后,正反应速率增大,则下列说法正确的是( ) A.A.的转化率增大B.平衡向逆向移动 C.平衡没有移动D.上述三种情况都有可能
第4 min至第6 min该化学反应处于平衡状态 第2 min时,如果只改变某一条件,则改变的条件可能是降低温度 第2 min时,如果只改变某一条件,则改变的条件可能是使用催化剂 第6 min时,其他条件不变,如果升高温度,正反应速率增大

 )减小 通入少量HCl,溶液漂白性增强 加入少量固体NaOH,一定有c(Na+)=c(
)减小 通入少量HCl,溶液漂白性增强 加入少量固体NaOH,一定有c(Na+)=c(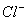 )+c(
)+c( ) 加入少量水,水的电离平衡向正反应方向移动
) 加入少量水,水的电离平衡向正反应方向移动
 减小 通入少量SO2,溶液漂白性增强 加入少量固体NaOH,一定有c(Na+)=c(Cl-)+c(ClO-) 加入少量水,水的电或平衡向正反应方向移动
减小 通入少量SO2,溶液漂白性增强 加入少量固体NaOH,一定有c(Na+)=c(Cl-)+c(ClO-) 加入少量水,水的电或平衡向正反应方向移动
 p (g)+q (g),在密闭容器中反应达到平衡,改变某一条件后,正反应速率增大,则下列说法正确的是( ) A.A.的转化率增大B.平衡向逆向移动 C.平衡没有移动D.上述三种情况都有可能
p (g)+q (g),在密闭容器中反应达到平衡,改变某一条件后,正反应速率增大,则下列说法正确的是( ) A.A.的转化率增大B.平衡向逆向移动 C.平衡没有移动D.上述三种情况都有可能