你可能感兴趣的试题
Ca2+含量 Ca2+和Mg2+总量 Mg2+含量 溶液中阳离子总量
Fe3O4溶于足量稀HNO3:Fe3O4+8H+=Fe2++2Fe3++4H2O 等物质的量的MgCl2、Ba(OH)2 和 HC1 溶液混合:Mg2++2OH-= Mg(OH)2↓ 将过量的SO2通入Ca(ClO)2溶液中: SO2+ClO-+H2O =HClO+ HSO3- 将0.2 mol·L-1的NH4Al(SO4)2溶液与0.3 mol·L-1的Ba(OH)2溶液等体积混合: 2Al3++3SO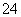 +3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓
+3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓
向FeCl2溶液中通入Cl2:Fe2++Cl2===Fe3++2Cl- 澄清石灰水与少量的小苏打溶液混合:Ca2++OH-+HCO ===CaCO3↓+H2O FeS固体放入稀硝酸溶液中:FeS+2H+===Fe2++H2S↑ AlCl3溶液中加过量氨水:Al3++4OH-===[Al(OH)4]-
===CaCO3↓+H2O FeS固体放入稀硝酸溶液中:FeS+2H+===Fe2++H2S↑ AlCl3溶液中加过量氨水:Al3++4OH-===[Al(OH)4]-
Fe3O4溶于足量稀HNO3:Fe3O4+8H+=Fe2++2Fe3++4H2O 等物质的量的MgCl2、Ba(OH)2 和 HC1 溶液混合:Mg2++2OH-= Mg(OH)2↓ 将过量的SO2通入Ca(ClO)2溶液中: SO2+ClO-+H2O =HClO+ HSO3- 将0.2 mol·L-1的NH4Al(SO4)2溶液与0.3 mol·L-1的Ba(OH)2溶液等体积混合: 2Al3++3SO +3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓
+3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓
Na、Mg、Al、Fe单质中只有Na能与水反应 Fe2O3 、Al2O3、MgO都是致密的氧化膜,能保护内层金属不被腐蚀 Fe(OH)3、 Al(OH)3都能与NaOH溶液反应 金属Na、Mg、Al、Fe都能和盐酸反应,生成氢气
Ca2+含量; Mg2+含量; Ca2+、Mg2+总量; Fe3+; Ca2+、Mg2+、Fe3+、Al3+总量
把Mg粉放入FeCl3溶液中: 2Fe3++ 3Mg+ 6H2O= 2Fe(OH)3↓+3 Mg2++3H2↑ 用漂白粉溶液吸收尾气中SO2:Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO 氯化铝溶液中加入偏铝酸钠溶液:Al3+ +3AlO2- +6H2O= 4Al(OH)3 ↓ 碳酸氢钙溶液中加入少量的氢氧化钠溶液:Ca2++2HCO3-+2OH-=CaCO3↓+2H2O+CO32-
向明矾溶液中滴加Ba(OH)2溶液,恰好使SO42-沉淀完全:2Al3++3SO42-+6OH-=2Al(OH)3↓+3BaSO4↓ (NH4)3Fe(SO4)3溶液与过量NaOH溶液反应: Fe3+ +2OH-=Fe(OH)3↓ 澄清石灰水这加入足量NaHCO3溶液:Ca2+ + 2OH- + 2HCO3- =CaCO3↓+ H2O+CO32- 向Mg(HCO3)2溶液中加入少量的NaOH溶液:Mg2++2HCO3-+4OH-=Mg(OH)2↓+2CO32-+2H2O
向FeCl3溶液中加入Mg(OH)2:3Mg(OH)2+2Fe3+=2Fe(OH)3+3Mg2+ 醋酸溶液与水垢中的CaCO3反应: CaCO3+2H+=Ca2++H2O+CO2↑ 向NaAIO2溶液中通入过量CO2制Al(OH)3:CO2+2AIO2-+3H2O=2Al(OH)3↓+CO32- 向Ba(OH)2溶液中滴加NaHSO4溶液至混合溶液恰好为中性:Ba2++OH-+H++SO42-=BaSO4↓+H2O
Fe2O3 [Al2O3]用盐酸 Fe(OH)3[Al(OH)3]用氨水 MgCl2[AlCl3]用氢氧化钠溶液 Mg [Al]用氢氧化钠溶液
Mg2+量 Ca2+量 Ca2+、Mg2+总量 Ca2+、Mg2+、Fe3+、Al3+总量
Mg2+的含量 Ca2+、Mg2+含量 Al3+、Fe3+的含量 Ca2+、Mg2+、Al3+、Fe3+的含量
该混合粉末从组成看,其成分皆是碱性氧化物 溶液Y中的阳离子主要是Mg2+、Al3+、Fe3+ 沉淀X的成分是SiO2 在溶液Y中加入过量的氨水,过滤得到的沉淀的成分是Fe(OH)3和Mg(OH)2

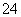 +3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓
+3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓
 ===CaCO3↓+H2O FeS固体放入稀硝酸溶液中:FeS+2H+===Fe2++H2S↑ AlCl3溶液中加过量氨水:Al3++4OH-===[Al(OH)4]-
===CaCO3↓+H2O FeS固体放入稀硝酸溶液中:FeS+2H+===Fe2++H2S↑ AlCl3溶液中加过量氨水:Al3++4OH-===[Al(OH)4]-
 +3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓
+3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓