你可能感兴趣的试题
x+y=z;a>0 x+y>z;a<0 x+yx+y0
该反应的化学方程式为:3X+2Y 2Z 若两容器中均达到平衡时,两容器的体积V.(Ⅰ)<V.(Ⅱ),则容器Ⅱ达到平衡所需时间大于t0 若两容器中均达到平衡时,两容器中Z.的物质的量分数相同,则Y.为固态或液态 若达平衡后,对容器Ⅱ升高温度时其体积增大,说明Z.发生的反应为吸热反应
2Z 若两容器中均达到平衡时,两容器的体积V.(Ⅰ)<V.(Ⅱ),则容器Ⅱ达到平衡所需时间大于t0 若两容器中均达到平衡时,两容器中Z.的物质的量分数相同,则Y.为固态或液态 若达平衡后,对容器Ⅱ升高温度时其体积增大,说明Z.发生的反应为吸热反应
(g)+y (g) z (g) ΔH.=a kJ•mol—1。将x molA.和y molB.混合在密闭容器中,在不同温度(T.1>T.2)及压强(P.1>P.2)下,C.的物质的量nC.与反应时间(t)的关系如图所示。下列判断正确的是( ) A.x+y=z;a>0B.x+y>z;a<0 C.x+yx+y0
z (g) ΔH.=a kJ•mol—1。将x molA.和y molB.混合在密闭容器中,在不同温度(T.1>T.2)及压强(P.1>P.2)下,C.的物质的量nC.与反应时间(t)的关系如图所示。下列判断正确的是( ) A.x+y=z;a>0B.x+y>z;a<0 C.x+yx+y0
在当温度不变,容器体积变为1L时,Z.的物质的量增大 在温度、体积不变的情况下,用Z.表示化学反应的速率为0.8 mol/L(L.・min) 在体积不变,升高温度重新达到平衡时,Z.的物质的量为1.4mol,则正反应是放热反应 在温度体积不变情况下,若再充入2 molX、1molY.,重新达平衡后,Z.的体积分数不变
(g)+y (g) z (g);△H=A.将x molA.和y molB.混合在密闭容器中,在不同温度(T1>T2)及压强(P1>P2)下,C的物质的量n(C)与反应时间(t)的关系如图所示.下列判断正确的是( ) 
A.x+y=z;a>0 B.x+y>z;a<0
C.x+y<z;a<0 x+y<z;a>0
T.1大于T.2 Y.一定呈气态 升高温度,该反应的化学平衡常数增大 当n(X):n(Y):n(Z)=1:3:2时,反应一定达到平衡状态 
同温同压同z时,加入催化剂,平衡时Q.的体积分数增加 同压同z时,升高温度,平衡时Q.的体积分数增加 同温同z时,增加压强,平衡时Q.的体积分数增加 同温同压时,增加z,平衡时Q.的体积分数增加
该反应的化学方程式为:3X+2Y  2Z 若两容器中均达到平衡后,两容器的体积V.(I.)0 若两容器中均达到平衡时,两容器中Z.的物质的量分数相同,则Y.为固态或液态 达平衡后,若对容器II升高温度时其体积增大,说明Z.发生的反应为吸热反应
2Z 若两容器中均达到平衡后,两容器的体积V.(I.)0 若两容器中均达到平衡时,两容器中Z.的物质的量分数相同,则Y.为固态或液态 达平衡后,若对容器II升高温度时其体积增大,说明Z.发生的反应为吸热反应
该反应的化学方程式为:3X+2Y 2Z 若两容器中均达到平衡时,两容器的体积V.(Ⅰ)<V.(Ⅱ), 则容器Ⅱ达到平衡所需时间小于t0 若两容器中均达到平衡时,两容器中Z.的物质的量分数相同,则Y.为固态或液态 若达平衡后,对容器Ⅱ升高温度时,其体积增大,说明Z.发生的反应为吸热反应
2Z 若两容器中均达到平衡时,两容器的体积V.(Ⅰ)<V.(Ⅱ), 则容器Ⅱ达到平衡所需时间小于t0 若两容器中均达到平衡时,两容器中Z.的物质的量分数相同,则Y.为固态或液态 若达平衡后,对容器Ⅱ升高温度时,其体积增大,说明Z.发生的反应为吸热反应
T.1大于T.2
Y.一定呈气态
升高温度,该反应的化学平衡常数增大
当n(X):n(Y):n(Z)=1:3:2时,反应一定达到平衡状态

该反应的化学方程式为:3X+2Y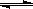 2Z 若两容器中均达到平衡时,两容器的体积V.(Ⅰ)<V.(Ⅱ),则容器Ⅱ达到平衡所需时间小于t0 若两容器中均达到平衡时,两容器中Z.的物质的量分数相同,则Y.为固态或液态 若达平衡后,对容器Ⅱ升高温度时其体积增大,说明Z.发生的反应为吸热反应
2Z 若两容器中均达到平衡时,两容器的体积V.(Ⅰ)<V.(Ⅱ),则容器Ⅱ达到平衡所需时间小于t0 若两容器中均达到平衡时,两容器中Z.的物质的量分数相同,则Y.为固态或液态 若达平衡后,对容器Ⅱ升高温度时其体积增大,说明Z.发生的反应为吸热反应
同温同压同z时,加入催化剂,平衡时 Q.的体积分数不改变 同温同压时,增加z,平衡时Q.的体积分 数一定增加 同温同z时,增加压强,平衡时Q.的体 积分数一定减小 同压同z时,升高温度,平衡时Q.的体积分数一定增加
同温同压同z时,加入催化剂,平衡时Q.的体积分数增加 同压同z时,升高温度,平衡时Q.的体积分数增加 同温同z时,增加压强,平衡时Q.的体积分数增加 同温同压时,增加z,平衡时Q.的体积分数增加
该反应的化学方程式为:3Z 3X+2Y t0时,X.、Y.、Z.的质量不再改变 t0时,Z.的浓度为1.2 mol/L t0时,反应停止,反应速率为0
3X+2Y t0时,X.、Y.、Z.的质量不再改变 t0时,Z.的浓度为1.2 mol/L t0时,反应停止,反应速率为0
升高温度,该反应的化学平衡常数增大 Y.一定呈气态 当c(X):c(Y):c(Z)=1:3:2时,反应达到平衡状态 T1大于T2

 2Z 若两容器中均达到平衡时,两容器的体积V.(Ⅰ)<V.(Ⅱ),则容器Ⅱ达到平衡所需时间大于t0 若两容器中均达到平衡时,两容器中Z.的物质的量分数相同,则Y.为固态或液态 若达平衡后,对容器Ⅱ升高温度时其体积增大,说明Z.发生的反应为吸热反应
2Z 若两容器中均达到平衡时,两容器的体积V.(Ⅰ)<V.(Ⅱ),则容器Ⅱ达到平衡所需时间大于t0 若两容器中均达到平衡时,两容器中Z.的物质的量分数相同,则Y.为固态或液态 若达平衡后,对容器Ⅱ升高温度时其体积增大,说明Z.发生的反应为吸热反应
 z (g) ΔH.=a kJ•mol—1。将x molA.和y molB.混合在密闭容器中,在不同温度(T.1>T.2)及压强(P.1>P.2)下,C.的物质的量nC.与反应时间(t)的关系如图所示。下列判断正确的是( ) A.x+y=z;a>0B.x+y>z;a<0 C.x+y
z (g) ΔH.=a kJ•mol—1。将x molA.和y molB.混合在密闭容器中,在不同温度(T.1>T.2)及压强(P.1>P.2)下,C.的物质的量nC.与反应时间(t)的关系如图所示。下列判断正确的是( ) A.x+y=z;a>0B.x+y>z;a<0 C.x+y

 2Z 若两容器中均达到平衡后,两容器的体积V.(I.)
2Z 若两容器中均达到平衡后,两容器的体积V.(I.) 2Z 若两容器中均达到平衡时,两容器的体积V.(Ⅰ)<V.(Ⅱ), 则容器Ⅱ达到平衡所需时间小于t0 若两容器中均达到平衡时,两容器中Z.的物质的量分数相同,则Y.为固态或液态 若达平衡后,对容器Ⅱ升高温度时,其体积增大,说明Z.发生的反应为吸热反应
2Z 若两容器中均达到平衡时,两容器的体积V.(Ⅰ)<V.(Ⅱ), 则容器Ⅱ达到平衡所需时间小于t0 若两容器中均达到平衡时,两容器中Z.的物质的量分数相同,则Y.为固态或液态 若达平衡后,对容器Ⅱ升高温度时,其体积增大,说明Z.发生的反应为吸热反应

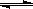 2Z 若两容器中均达到平衡时,两容器的体积V.(Ⅰ)<V.(Ⅱ),则容器Ⅱ达到平衡所需时间小于t0 若两容器中均达到平衡时,两容器中Z.的物质的量分数相同,则Y.为固态或液态 若达平衡后,对容器Ⅱ升高温度时其体积增大,说明Z.发生的反应为吸热反应
2Z 若两容器中均达到平衡时,两容器的体积V.(Ⅰ)<V.(Ⅱ),则容器Ⅱ达到平衡所需时间小于t0 若两容器中均达到平衡时,两容器中Z.的物质的量分数相同,则Y.为固态或液态 若达平衡后,对容器Ⅱ升高温度时其体积增大,说明Z.发生的反应为吸热反应
 3X+2Y t0时,X.、Y.、Z.的质量不再改变 t0时,Z.的浓度为1.2 mol/L t0时,反应停止,反应速率为0
3X+2Y t0时,X.、Y.、Z.的质量不再改变 t0时,Z.的浓度为1.2 mol/L t0时,反应停止,反应速率为0