
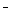 )=c(H
)=c(H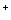 )+c(HB
)+c(HB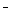 )+2c(H2B) NaHB溶液可能存在以下关系:c(Na
)+2c(H2B) NaHB溶液可能存在以下关系:c(Na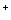 )>c(HB
)>c(HB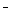 )>c(OH
)>c(OH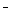 )>c(H
)>c(H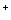 ) NaHB水溶液中一定有:c(Na
) NaHB水溶液中一定有:c(Na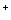 )+c(H
)+c(H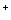 )=c(HB
)=c(HB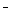 )+c(OH
)+c(OH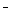 )+c(B
)+c(B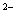 ) NaHB溶液一定呈酸性,Na2B溶液一定呈碱性
) NaHB溶液一定呈酸性,Na2B溶液一定呈碱性
 H3O+ +B2- 溶液中离子浓度大小为:c(Na+)>c(HB-)>c(OH-) >c(H+) NaHB的存在抑制了水的电离 相同物质的量浓度溶液的pH值:NaHB > Na2B
H3O+ +B2- 溶液中离子浓度大小为:c(Na+)>c(HB-)>c(OH-) >c(H+) NaHB的存在抑制了水的电离 相同物质的量浓度溶液的pH值:NaHB > Na2B
 )=c(H
)=c(H )+c(HB
)+c(HB )+2c(H2B) NaHB溶液可能存在以下关系:c(Na
)+2c(H2B) NaHB溶液可能存在以下关系:c(Na )>c(HB
)>c(HB )>c(OH
)>c(OH )>c(H
)>c(H ) NaHB水溶液中一定有:c(Na
) NaHB水溶液中一定有:c(Na )+c(H
)+c(H )=c(HB
)=c(HB )+c(OH
)+c(OH )+c(B
)+c(B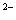 ) NaHB溶液一定呈酸性,Na2B溶液一定呈碱性
) NaHB溶液一定呈酸性,Na2B溶液一定呈碱性
 H3O+ +B2- 溶液中离子浓度大小为:c(Na+)>c(HB-)>c(OH-) >c(H+) NaHB的存在抑制了水的电离 相同物质的量浓度溶液的pH值:NaHB > Na2B
H3O+ +B2- 溶液中离子浓度大小为:c(Na+)>c(HB-)>c(OH-) >c(H+) NaHB的存在抑制了水的电离 相同物质的量浓度溶液的pH值:NaHB > Na2B
 H3O++B2– 电解饱和食盐水: 1-+2H2O
H3O++B2– 电解饱和食盐水: 1-+2H2O H2↑+Cl2↑+OH- C. 氢氧燃料电池在碱性介质中的正极反应式:O2+2H2O+4e一=4OH- FeBr2溶液中通入过量Cl2:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl-
H2↑+Cl2↑+OH- C. 氢氧燃料电池在碱性介质中的正极反应式:O2+2H2O+4e一=4OH- FeBr2溶液中通入过量Cl2:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl-
溶液中离子浓度大小为:c(Na+)=c(HB﹣)>c(OH﹣)=c(H+)
NaHB的存在抑制了水的电离
相同物质的量浓度溶液的pH:Na2B>NaHB
 H3O++B2– 电解饱和食盐水: 1-+2H2O
H3O++B2– 电解饱和食盐水: 1-+2H2O H2↑+Cl2↑+OH- C. 氢氧燃料电池在碱性介质中的正极反应式:O2+2H2O+4e一=4OH- FeBr2溶液中通入过量Cl2:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl-
H2↑+Cl2↑+OH- C. 氢氧燃料电池在碱性介质中的正极反应式:O2+2H2O+4e一=4OH- FeBr2溶液中通入过量Cl2:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl-