
 、Cl- Mg2+、NH
、Cl- Mg2+、NH 、SO
、SO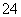 、NO
、NO H.+、K.+、Cl-、CH3COO- Fe3+、K.+、AlO
H.+、K.+、Cl-、CH3COO- Fe3+、K.+、AlO 、SO
、SO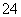
 、Cl- Cu2+、K+、
、Cl- Cu2+、K+、 、
、 H+、K+、
H+、K+、 、Cl- Mg2+、Na+、Cl-、
、Cl- Mg2+、Na+、Cl-、
 、NO
、NO Na+、AlO
Na+、AlO 、HCO
、HCO 、K.+ ClO-、I.-、NH
、K.+ ClO-、I.-、NH 、Ba2+ Na+、SO
、Ba2+ Na+、SO 、Mg2+、Cl-
、Mg2+、Cl-
 、Cl- Mg2+、NH
、Cl- Mg2+、NH 、SO
、SO 、NO
、NO H.+、K.+、Cl-、CO32- K.+、Ca2+、CO
H.+、K.+、Cl-、CO32- K.+、Ca2+、CO 、OH-
、OH-
 、Cl- K.+、Mg2+、CO
、Cl- K.+、Mg2+、CO 、OH- H.+、K.+、Cl-、CH3COO- Mg2+、NH
、OH- H.+、K.+、Cl-、CH3COO- Mg2+、NH 、SO
、SO 、NO
、NO