你可能感兴趣的试题
四种溶液的pH大小顺序是③>②>①>④ 若分别加入25mL 0.1mol·L-1盐酸充分反应后,pH最大的是① 若将四种溶液稀释相同倍数,pH变化最大的是④ 升高温度,四种溶液的pH均减小
NaHCO3溶液中,一定有c(Na+)=c(HCO3-)+c(CO32-) 1 mol·L-1HCN溶液与1mol·L-1 NaOH溶液等体积混合后,测得所得溶液显酸性 等物质的量浓度的各溶液pH关系为:pH(Na2CO3)>pH(NaCN)>pH(CH3COONa) 1mol/L.醋酸溶液加水稀释,所有离子浓度均减小
0.1mol·L-1Na2CO3溶液中:c(OH-)=c(HCO3-)+c(H+)+c(H2CO3) 0.1mol·L-1CH3COONa溶液中:c(Na+)=c(CH3COO-)+c(OH-) 浓度均为0.1mol·L-1的CH3COONa、NaOH和Na2CO3三种溶液的pH大小顺序: pH(NaOH)>pH(Na2CO3)>pH(CH3COONa) 向0.1mol·L-1CH3COOH溶液中滴加NaOH溶液至中性,溶液中离子浓度的关系: c(CH3COO-)>c(Na+)>c(OH-)=c(H+)
0.1mol・L-1Na2CO3溶液中:c(OH-)=c(HCO3-)+c(H+)+c(H2CO3) 0.1mol・L-1CH3COONa溶液中:c(Na+)=c(CH3COO-)+c(OH-) 浓度均为0.1mol・L-1的CH3COONa、NaOH和Na2CO3三种溶液的pH大小顺序: pH(NaOH)>pH(Na2CO3)>pH(CH3COONa) 向0.1mol・L-1CH3COOH溶液中滴加NaOH溶液至中性,溶液中离子浓度的关系: c(CH3COO-)>c(Na+)>c(OH-)=c(H+)
CH3COONa NaClO Na2CO3 Na3PO4
3种溶液pH的大小顺序是③>②>① 若将3种溶液稀释相同倍数,pH变化最大的是② 若分别加入25 mL 0.1 mol·L-1的盐酸后,pH最大的是① 若3种溶液的pH均为9,则物质的量浓度的大小顺序是③>①>②
各溶液pH关系为:pH(Na2CO3)>pH(NaCN)>pH(CH3COONa) a mol·L-1HCN溶液与b mol·L-1NaOH溶液等体积混合,所得溶液中c(Na+)>c(CN-),则a一定小于b 冰醋酸中逐滴加水,则溶液的导电性和pH均先增大后减小 NaHCO3和Na2CO3混合溶液中,一定有2c(Na+)=3〔c(H2CO3)+c(HCO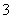 )+c(CO
)+c(CO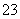 )〕
)〕
pH=2的HA溶液与pH=12的MOH溶液任意比混合: c(H+) + c(M+) === c(OH-) + c(A-) pH相等的CH3COONa、NaOH和Na2CO3三种溶液: c(NaOH)<c(CH3CO ONa)<c(Na2CO3) 物质的量浓度相等CH3COOH和CH3COONa溶液等体积混合: c(CH3COO-) +2c(OH-) === c(H+) + c(CH3COOH) 0.1mol•L-1的NaHA溶液,其pH=4:c(HA-)>c(H+)>c(H2A)>c(A2-)
各溶液pH关系为:pH(Na2CO3)>pH(NaCN)>pH(CH3COONa) a mol·L-1HCN溶液与b mol·L-1NaOH溶液等体积混合,所得溶液中c(Na+)>c(CN-),则a一定小于b 冰醋酸中逐滴加水,则溶液的导电性和pH均先增大后减小 NaHCO3和Na2CO3混合溶液中,一定有2c(Na+)=3〔c(H2CO3)+c(HCO )+c(CO
)+c(CO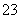 )〕
)〕
pH相等的CH3COONa、NaOH和Na2CO3三种溶液:c(NaOH)<c(Na2CO3)<c(CH3COONa) pH=5的下列溶液(①NH4Cl溶液;②CH3COOH溶液;③稀盐酸)中c(H+)水:①>②>③ pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合后,滴入石蕊溶液呈红色 0.1 mol/L的醋酸溶液的pH=a,0.01 mol/L的醋酸溶液的pH=b,则b<a+1
与HCl加成生成CH3COCl 与H2O加成生成CH3COOH 与CH3OH加成生成CH3COCH2OH 与CH3COOH加成生成(CH3CO)2O
3种溶液pH的大小顺序是 ③>②>① 若将3种溶液稀释相同倍数,pH变化最大的是② 若分别加入25mL0.1mol·L-1盐酸后,pH最大的是① 若3种溶液的pH均为9,则物质的量浓度的大小顺序是③>①>②
等物质的量浓度的各溶液pH关系为pH(NaCN)>pH(Na2CO3)>pH(CH3COONa) amol·L—1HCN溶液与amol·L—1NaOH溶液等体积混合后,所得溶液显碱性(pH>7),则c (OH-)>c(H+),c(Na+)>c(CN-) 冰醋酸中逐滴加水,溶液的导电性、醋酸的电离程度、pH均先增大后减小 NaHCO3和Na2CO3混合溶液中,一定有c(Na+)+c(H+)=c(OH-)+c(HCO3-) +c(CO )
)
碳酸溶液中, 第一级电离出的的2倍 在Na2CO3和NaHCO3的混合溶液中:c(Na+)+c(H+)=c(HCO3-)+c(OH-)+c(C032-) 25。C.时,pH=10的CH3COONa溶液与pH=l0的氨水中,由水电离出的c(OH-) 之比为1:1 物质的量浓度相同的4种溶液①CH3COONa ②NaNO3 ③Na2CO3 ④NaOH,pH的大小顺序是④>③>①>②
第一级电离出的的2倍 在Na2CO3和NaHCO3的混合溶液中:c(Na+)+c(H+)=c(HCO3-)+c(OH-)+c(C032-) 25。C.时,pH=10的CH3COONa溶液与pH=l0的氨水中,由水电离出的c(OH-) 之比为1:1 物质的量浓度相同的4种溶液①CH3COONa ②NaNO3 ③Na2CO3 ④NaOH,pH的大小顺序是④>③>①>②
0.1 mol·L-1的CH3COOH溶液中,由水电离的c(H+)为10-13 mol·L-1 pH=2与pH=1的CH3COOH溶液中c(H+)之比为1︰10 等体积pH=12的NaOH溶液和pH=2的CH3COOH溶液混合,混合后溶液pH<7
1.0 mol·L-1Na2CO3溶液:c(OH-)=c(HCO3-)+c(H+)+2c(H2CO3)

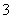 )+c(CO
)+c(CO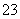 )〕
)〕
 )+c(CO
)+c(CO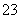 )〕
)〕
 )
)
 第一级电离出的的2倍 在Na2CO3和NaHCO3的混合溶液中:c(Na+)+c(H+)=c(HCO3-)+c(OH-)+c(C032-) 25。C.时,pH=10的CH3COONa溶液与pH=l0的氨水中,由水电离出的c(OH-) 之比为1:1 物质的量浓度相同的4种溶液①CH3COONa ②NaNO3 ③Na2CO3 ④NaOH,pH的大小顺序是④>③>①>②
第一级电离出的的2倍 在Na2CO3和NaHCO3的混合溶液中:c(Na+)+c(H+)=c(HCO3-)+c(OH-)+c(C032-) 25。C.时,pH=10的CH3COONa溶液与pH=l0的氨水中,由水电离出的c(OH-) 之比为1:1 物质的量浓度相同的4种溶液①CH3COONa ②NaNO3 ③Na2CO3 ④NaOH,pH的大小顺序是④>③>①>②