你可能感兴趣的试题
原电池工作时H+在铜电极被氧化成H2 原电池工作时Zn发生氧化反应 原电池工作时SO42-移向铜极 原电池工作时电子通过电解质由Zn流向Cu
Zn 碳棒 MnO2和NH4+ Zn 2+和NH4+
碳为电池的负极 Zn极上发生氧化反应 电流由锌极流向碳极 H2在Zn片上生成 
干电池中Zn为正极,碳为负极 干电池工作时,电子由Zn极经外电路流向碳极 干电池长时间连续使用时内装糊状物可能流出腐蚀电器 干电池可以实现化学能向电能的转化和电能向化学能的转化
干电池中Zn为正极,碳为负极 干电池工作时,电流由Zn极经外电路流向碳极 干电池长时间连续使用时内装糊状物可能流出腐蚀电器 干电池可以实现化学能向电能的转化和电能向化学能的转化
干电池中锌筒为正极,石墨棒为负极 干电池长时间连续工作后,糊状物可能流出,腐蚀用电器 干电池工作时,电流方向是由锌筒经外电路流向石墨棒 干电池可实现电能向化学能的转化
负极反应为Zn-2e-=Zn2+ 负极反应为Zn+2H2O-2e-= Zn(OH)2+H+ 正极反应为2MnO2+2H++ 2e-=2MnOOH 正极反应为2MnO2+2H2O + 2e-=2MnOOH+2OH-
Cu电极为正极 原电池工作时,电子从Zn电极流出 原电池工作时的总反应为:Zn+Cu2+=Zn2++Cu 盐桥(琼脂-饱和KCl溶液)中的K.+移向ZnSO4溶液
Zn 碳棒 MnO2和NH4+ Zn 2+和NH4+
Zn 碳棒 MnO2和NH4+ Zn 2+和NH4+
Zn为正极,碳棒为负极 工作时,电子由Zn极经电解质溶液流向碳极 电池的正极反应为2NH +2e-= 2NH3↑+H2↑ 长时间使用该电池,可能发生胀气和漏液
+2e-= 2NH3↑+H2↑ 长时间使用该电池,可能发生胀气和漏液
干电池工作时,电流方向由石墨棒经外电路流向锌筒 干电池在使用过程中,锌会逐渐溶解 若用湿的KOH替代电解质NH4Cl,可延长电池寿命和提高电池性能 干电池可实现化学能与电能的相互转化
Zn为正极,碳棒为负极 工作时,电子由Zn极经电解质溶液流向碳极 电池的正极反应为2NH+2e-= 2NH3↑+H2↑ 长时间使用该电池,可能发生胀气和漏液
最早使用的化学电池是锌锰电池,它是一次性电池 电池使用过程中,锌会逐渐溶解:Zn=Zn2++2e﹣ 锌锰电池即使不用,放置过久,也会失效 锌锰干电池内的电解质NH4Cl可以换成HCl溶液 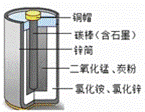
Cu电极为正电极 原电池工作时,电子从Zn电极流出 原电池工作时的总反应为:Zn+Cu2+=Zn2++Cu 盐桥(琼脂-饱和KCl溶液)中的K.+移向ZnSO4溶液
负极反应为Zn-2e-==Zn2+ 负极反应为Zn+2H2O-2e-==Zn(OH)2+H+ 正极反应为2MnO2+2H++2e-==2MnOOH 正极反应为2MnO2+2H2O+2e-==2MnOOH+2OH-


 +2e-= 2NH3↑+H2↑ 长时间使用该电池,可能发生胀气和漏液
+2e-= 2NH3↑+H2↑ 长时间使用该电池,可能发生胀气和漏液
